[Lý thuyết Hóa Lớp 10] Mô hình nguyên tử
Hướng dẫn học bài: Mô hình nguyên tử - Môn Hóa học Lớp 10 Lớp 10. Đây là sách giáo khoa nằm trong bộ sách 'Lý thuyết Hóa Lớp 10 Lớp 10' được biên soạn theo chương trình đổi mới của Bộ giáo dục. Hi vọng, với cách hướng dẫn cụ thể và giải chi tiết các bé sẽ nắm bài học tốt hơn.
mô hình rutherford – bohr có nội dung gì?
mô hình rutherford – bohr có 3 nội dung chính
1. khối lượng nguyên tử tập trung chủ yếu ở hạt nhân
2. electron quay xung quanh hạt nhân theo quỹ đạo giống nư hành tinh quay xung quanh mặt trời
3. năng lượng electron phụ thuộc vào khoảng cách từ electron đó tới hạt nhân nguyên tử. electron ở càng xa hạt nhân thì có năng lượng càng cao
ví dụ:
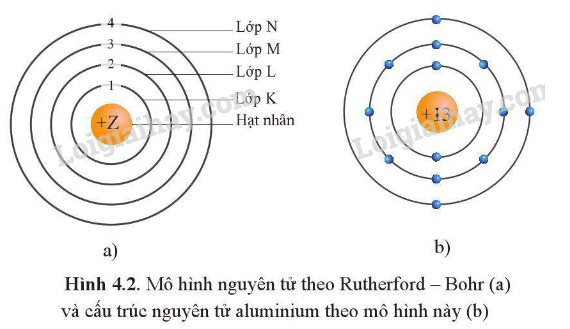
lớp electron được phân chia như thế nào?
lớp thứ 1 gọi là lớp k có tối đa 2n2 (với n là số lớp)
lớp thứ 2 gọi là lớp l có tối đa 2n2 (với n là số lớp)
lớp thứ 3 gọi là lớp m có tối đa 2n2 (với n là số lớp)
lớp thứ 4 gọi là lớp n có tối đa 2n2 (với n là số lớp)
mô hình hiện đại về nguyên tử khác mô hình nguyên tử rutherford – bohr ở đâu?
các điểm khác nhau:
1. các electron chuyển động xung quanh hạt nhân không theo những quỹ đạo xác định.
2. electron chuyển động rất nhanh trong cả khu vực không gian với xác suất tìm thấy khác nhau tạo thành những hình ảnh giống như đám mây electron
ví dụ: