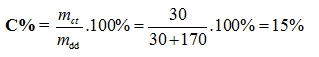[Trắc nghiệm KHTN Lớp 8 Cánh diều] Trắc nghiệm Bài 9: Base Khoa học tự nhiên 8 Cánh diều có đáp án
Hướng dẫn học bài: Trắc nghiệm Bài 9: Base Khoa học tự nhiên 8 Cánh diều có đáp án - Môn Khoa học tự nhiên Lớp 8 Lớp 8. Đây là sách giáo khoa nằm trong bộ sách 'Trắc nghiệm KHTN Lớp 8 Cánh diều Lớp 8' được biên soạn theo chương trình đổi mới của Bộ giáo dục. Hi vọng, với cách hướng dẫn cụ thể và giải chi tiết các bé sẽ nắm bài học tốt hơn.
Đề bài
Tên gọi của NaOH là:
Có thể nhận biết các dung dịch: NaOH, HCl, H2O đây bằng cách nào?
Phản ứng nào sau đây đúng?
Tính thể tích của dung dịch H2SO4 0,4M cần dùng để phản ứng hết với 100ml dung dịch NaOH 0,2 M?
Trong sản xuất nhôm có giai đoạn nhiệt phân Al(OH)3 để thu được Al2O3. Phản ứng nhiệt phân xảy ra như sau: \(Al{(OH)_3} \to A{l_2}{O_3} + 3{H_2}O\)
Để thu được 1 tấn Al2O3 thì cần bao nhiêu tấn Al(OH)3, biết hiệu suất phản ứng đạt 90% (các giá trị được làm tròn đến hàng trăm)
Nhỏ từ từ dung dịch HCl 1M vào 100g dung dịch kiềm M(OH)n có nồng độ 1,71%. Để M(OH)n phản ứng hết thì cần dùng 20ml dung dịch HCl. Xác định kim loại trong hydroxide biết rằng hóa trị của kim loại có thể là I, II hoặc III
Để điều chế dung dịch nước vôi trong người ta cho calcium oxide tác dụng với nước. Phản ứng xảy ra như sau: CaO + H2O 🡪 Ca(OH)2
Cho 0,28g CaO tác dụng hoàn toàn với 100g nước. Nồng độ C% của dung dịch Ca(OH)2 thu được:
Có thể dùng chất nào sau đây để khử độ chua của đất?
Nhỏ dung dịch phenolphtalein vào hai dung dịch không màu X và Y thấy dung dịch X không thay đổi màu còn dung dịch Y chuyển sang màu hồng. Kết luận nào sau đây về dung dịch X và Y là đúng?
Dung dịch NaOH có thể tác dụng với dung dịch nào sau đây
Dãy chất nào sau đây chỉ gồm các base tan?
Cặp chất không thể tồn tại trong một dung dịch (tác dụng được với nhau) là:
Phương trình nào sau đây là sai?
Cặp chất đều làm đục nước vôi trong Ca(OH)2
Cặp chất khi phản ứng với nhau tạo thành chất kết tủa trắng:
Hòa tan 30 g NaOH vào 170 g nước thì thu được dung dịch NaOH có nồng độ là:
Hòa tan 80 g NaOH vào nước thu được dung dịch có nồng độ 1M. Thể tích dung dịch NaOH là:
Cho 200ml dung dịch NaOH 3M tác dụng với 100ml dung dịch FeCl3 1M thu được a gam kết tủa. Giá trị của a là :
Trộn 200ml dung dịch NaOH 1M với 300ml dung dịch NaOH 0,5M thì thu được dung dịch mới có nồng độ mol là?
Để trung hòa V ml dung dịch NaOH nồng độ 1,0M cần 200 ml dung dịch H2SO4 nồng độ 1,5M. Giá trị của V là
Trung hòa 200 gam dung dịch NaOH 10% bằng dung dịch HCl 3,65%. Khối lượng dung dịch HCl cần dùng là
200 gam
300 gam
400 gam
500 gam
Lời giải và đáp án
Tên gọi của NaOH là:
Đáp án : C
Dựa vào danh pháp quốc tế IUPAC
Đáp án C
Có thể nhận biết các dung dịch: NaOH, HCl, H2O đây bằng cách nào?
Đáp án : A
Các dung dịch đã cho có pH khác nhau nên có thể dùng chất chỉ thị để phân biệt
Đáp án A
Phản ứng nào sau đây đúng?
Đáp án : B
Dựa vào các hệ số cân bằng và hóa trị của nguyên tố trong các phản ứng
Đáp án B
Tính thể tích của dung dịch H2SO4 0,4M cần dùng để phản ứng hết với 100ml dung dịch NaOH 0,2 M?
Đáp án : A
Dựa vào tính chất hóa học của base.
Số mol của NaOH là: nNaOH = 0,2 x 0,1 = 0,02 (mol).
Phương trình hóa học: 2NaOH + H2SO4 🡪 Na2SO4 + 2H2O
0,02 --> 0,01
CM = n : V => V = n : CM = 0,01 : 0,4 = 0,025 lít
Từ đó, tính được thể tích dung dịch H2SO4 0,4 M cần dùng là 25ml
Trong sản xuất nhôm có giai đoạn nhiệt phân Al(OH)3 để thu được Al2O3. Phản ứng nhiệt phân xảy ra như sau: \(Al{(OH)_3} \to A{l_2}{O_3} + 3{H_2}O\)
Để thu được 1 tấn Al2O3 thì cần bao nhiêu tấn Al(OH)3, biết hiệu suất phản ứng đạt 90% (các giá trị được làm tròn đến hàng trăm)
Đáp án : A
Tính số mol của Al2O3, dựa vào hiệu suất của phản ứng
\({n_{A{l_2}{O_3}}} = \frac{{{{10}^6}}}{{102}}mol\)
Theo PTHH: 2Al(OH)3 🡪 Al2O3 + 3H2O
Số mol: \(\frac{{{{10}^6}}}{{51}}\) \( \leftarrow \frac{{{{10}^6}}}{{102}}\)
Vì hiệu suất phản ứng đạt 90% nên mAl(OH)3 = \(\frac{{{{10}^6}}}{{51}}x102:90\% = 1700400(g) \approx 1,7\tan \)
Nhỏ từ từ dung dịch HCl 1M vào 100g dung dịch kiềm M(OH)n có nồng độ 1,71%. Để M(OH)n phản ứng hết thì cần dùng 20ml dung dịch HCl. Xác định kim loại trong hydroxide biết rằng hóa trị của kim loại có thể là I, II hoặc III
Đáp án : A
Dựa vào số mol của dung dịch HCl
\({n_{HCl}} = {C_M}.{V_{HCl}} = 0,02x1 = 0,02mol\)
HCl + M(OH)n 🡪 MCln + nH2O
0,02 🡪 \(\frac{{0,02}}{n}\)
Khối lượng của M(OH)n đã phản ứng: \({m_{Mg(OH)2}} = {m_{{\rm{dd}}}}.\frac{{C\% }}{{100}} = 100.\frac{{1,71}}{{100}} = 1,71g\)
Ta có: \(\begin{array}{l}\frac{{0,02}}{n}.({M_M} + 17n) = 1,71\\ \to 0,02{M_M} = 1,37n\end{array}\)
Vì M có hóa trị I, II hoặc III. Thay n = 1, 2, 3 vào phương trình ta được: n = 2 và M = 137 (Ba)
Để điều chế dung dịch nước vôi trong người ta cho calcium oxide tác dụng với nước. Phản ứng xảy ra như sau: CaO + H2O 🡪 Ca(OH)2
Cho 0,28g CaO tác dụng hoàn toàn với 100g nước. Nồng độ C% của dung dịch Ca(OH)2 thu được:
Đáp án : C
Dựa vào công thức tính C%
nCaO = 0,005 mol
n CaO = n Ca(OH)2 = 0,005 mol
m Ca(OH)2 = 0,005 . 74 = 0,37%
m dung dịch = 100 + 0,28 = 100,28g
\(C\% = \frac{{37}}{{100,28}}.100 = 36,9\% \)
Có thể dùng chất nào sau đây để khử độ chua của đất?
Đáp án : A
Để khử độ chua của đất ta dùng các dung dịch có tính base
Đáp án A
Nhỏ dung dịch phenolphtalein vào hai dung dịch không màu X và Y thấy dung dịch X không thay đổi màu còn dung dịch Y chuyển sang màu hồng. Kết luận nào sau đây về dung dịch X và Y là đúng?
Đáp án : D
Dựa vào tính chất hóa học của base.
Base làm dung dịch phenolphtalein chuyển sang màu hồng
Dung dịch NaOH có thể tác dụng với dung dịch nào sau đây
Đáp án : C
Dựa vào tính chất hóa học của dung dịch base
Đáp án: C
Dãy chất nào sau đây chỉ gồm các base tan?
Đáp án : A
Dựa vào độ tan của các chất base.
Mg(OH)2 và Cu(OH)2 là hai base không tan.
Đáp án: A
Cặp chất không thể tồn tại trong một dung dịch (tác dụng được với nhau) là:
Đáp án : A
Cặp chất có tác dụng với nhau sinh ra chất mới thì không thể cùng tồn tại được với nhau trong một dung dịch.
Cặp chất không thể tồn tại trong một dung dịch (tác dụng được với nhau) là: Ca(OH)2, Na2CO3 vì xảy ra phản ứng:
Ca(OH)2 + Na2CO3 → CaCO3 ↓ + 2NaOH
Phương trình nào sau đây là sai?
Đáp án : A
Dựa vào tính chất hóa học của bazơ tan và không tan.
A. Sai, sửa: 2Fe(OH)3 \(\xrightarrow{{{t^0}}}\) Fe2O3 + 3H2O
B,C,D đúng
Cặp chất đều làm đục nước vôi trong Ca(OH)2
Đáp án : B
Dựa vào tính chất hóa học của dd Ca(OH)2
CO2 và SO2 làm đục dung dịch Ca(OH)2 do sinh ra CaCO3, CaSO3 kết tủa.
PTHH: Ca(OH)2 + CO2 → CaCO3↓ + H2O
Ca(OH)2 + SO2 → CaSO3↓ + H2O
Cặp chất khi phản ứng với nhau tạo thành chất kết tủa trắng:
Đáp án : A
Chọn cặp chất có tác dụng với nhau sinh ra sản phẩm muối kết tủa trắng.
A. Thỏa mãn vì phản ứng được với nhau sinh ra kết tủa trắng.
PTHH: Ca(OH)2 + Na2SO3 → CaSO3↓ + 2NaOH
B,C,D loại vì không xảy ra phản ứng
Hòa tan 30 g NaOH vào 170 g nước thì thu được dung dịch NaOH có nồng độ là:
Đáp án : C
Ghi nhớ công thức tính nồng độ phần trăm: \(C\% = \frac{{mc\tan }}{{m\,dd}}.100\% \)
mdd = m nước + mNaOH = 170 + 30 = 200g
![]()
Hòa tan 80 g NaOH vào nước thu được dung dịch có nồng độ 1M. Thể tích dung dịch NaOH là:
Đáp án : B
Ghi nhớ công thức tính nồng độ mol:\({C_M} = \frac{{{n_{NaOH}}}}{V} \to V = ?\)
nNaOH = mNaOH : MNaOH = 80 : (23 + 16 + 1) = 2 mol
VNaOH = nNaOH : CM NaOH = 2 : 1 = 2 lít
Cho 200ml dung dịch NaOH 3M tác dụng với 100ml dung dịch FeCl3 1M thu được a gam kết tủa. Giá trị của a là :
Đáp án : C
Đổi số mol NaOH; FeCl3
Viết PTHH xảy ra: 3NaOH + FeCl3 → 3NaCl + Fe(OH)3
Dựa vào PTHH so sánh NaOH và FeCl3 chất nào phản ứng hết, chất nào dư. Mọi tính toán theo số mol của chất phản ứng hết.
Số mol của NaOH là 0,2.3=0,6 mol
số mol của FeCl3 là 0,1.1=0,1mol
Ta có PTHH : 3NaOH + FeCl3 → 3NaCl + Fe(OH)3
Trước PƯ 0,6 mol 0,1 mol
PƯ 0,3 mol 0,1 mol
Sau PƯ 0,3 mol 0 0,1 mol
Kết tủa là 0,1 mol Fe(OH)3 => a= 0,1.107=10,7(g)
Trộn 200ml dung dịch NaOH 1M với 300ml dung dịch NaOH 0,5M thì thu được dung dịch mới có nồng độ mol là?
Đáp án : D
Công thức nồng độ mol: CM NaOH = nNaOH : VNaOH
Tống số mol NaOH có trong cả 2 dung dịch là
nNaOH = 0,2.1+ 0,3.0,5= 0,35 mol
Nồng độ mol của dung dịch thu được là
\({C_M}NaOH = \frac{{0,35}}{{0,5}} = 0,7\,(M)\)
Để trung hòa V ml dung dịch NaOH nồng độ 1,0M cần 200 ml dung dịch H2SO4 nồng độ 1,5M. Giá trị của V là
Đáp án : A
Bước 1: Đổi số mol H2SO4 theo công thức: nH2SO4 = VH2SO4 × CM H2SO4
Bước 2: Viết PTHH xảy ra, tính số mol NaOH theo số mol H2SO4
Bước 3: Tính VNaOH = nNaOH : CM NaOH = ?
200 ml = 0,2 (lít) ⟹ nH2SO4 = VH2SO4 × CM H2SO4 = 0,2 × 1,5 = 0,3 (mol)
PTHH: 2NaOH + H2SO4 → Na2SO4 + 2H2O
Theo PTHH: nNaOH = 2nH2SO4 = 2.0,3 = 0,6 (mol)
⟹ VNaOH = nNaOH : CM NaOH = 0,6 : 1,0 = 0,6 (lít) = 600 (ml)
⟹ V = 600 ml
Trung hòa 200 gam dung dịch NaOH 10% bằng dung dịch HCl 3,65%. Khối lượng dung dịch HCl cần dùng là
200 gam
300 gam
400 gam
500 gam
Đáp án : D
NaOH + HCl → NaCl + H2O
0,5 → 0,5 mol
+) tính mHCl $ = > {m_{dd\,\,HCl}}$
${m_{NaOH}} = \frac{{200.10\% }}{{100\% }} = 20\,\,gam\,\, = > \,\,{n_{NaOH}} = 0,5\,\,mol$
NaOH + HCl → NaCl + H2O
0,5 → 0,5 mol
=> mHCl = 0,5.36,5 = 18,25 gam $ = > {m_{dd\,\,HCl}} = \frac{{18,25.100\% }}{{3,65\% }} = 500\,\,gam$