Chuyên đề KHTN 8 Chân trời sáng tạo bài 3 Phản ứng hoá học và năng lượng trong các phản ứng được soạn dưới dạng file word và PDF gồm 9 trang. Các bạn xem và tải về ở dưới.
BÀI 3: PHẢN ỨNG HOÁ HỌC VÀ NĂNG LƯỢNG TRONG CÁC PHẢN ỨNG HOÁ HỌC
A. TÓM TẮT LÝ THUYẾT
1) Phản ứng hóa học
– Quá trình biến đổi chất này thành chất khác được gọi là phản ứng hóa học. Chất tham gia phản ứng gọi là chất đầu, chất mới tạo thành gọi là sản phẩm.
2) Diễn biến của phản ứng hóa học
– Trong phản ứng hóa học, có sự phá vỡ liên kết cũ và hình thành liên kết mới. Kết quả là chất này biến đổi thành chất khác.
3) Một số dấu hiệu nhận biết có phản ứng hóa học xảy ra
– Một số dấu hiệu có thể nhận biết phản ứng hóa học xảy ra: xuất hiện chất khí, chất kết tủa; thay đổi màu sắc, mùi; phát sáng, giải phóng hoặc hấp thụ nhiệt năng;…
4) Năng lượng trong phản ứng hóa học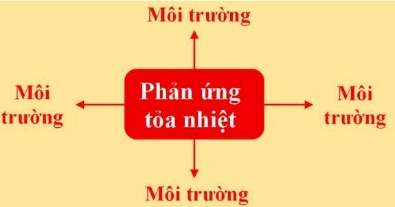
– Phản ứng tỏa nhiệt là phản ứng hóa học kèm theo sự giải phóng nhiệt năng ra môi trường.
Tổng quát:
Chất phản ứng → sản phẩm + năng lượng
– 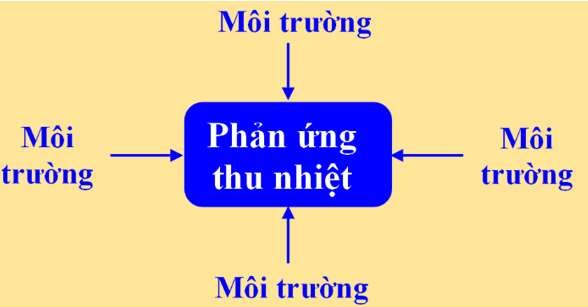 Phản ứng thu nhiệt là phản ứng hóa học nhận năng lượng từ môi trường xung quanh.
Phản ứng thu nhiệt là phản ứng hóa học nhận năng lượng từ môi trường xung quanh.
Tổng quát:
Chất phản ứng + năng lượng → sản phẩm
– Khi đốt cháy than, xăng, dầu, … sẽ tỏa ra một lượng nhiệt lớn, đây chính là phản ứng tỏa nhiệt. Lượng nhiệt này sẽ phục vụ cho các hoạt động trong đời sống và sản xuất của con người.
B. CÂU HỎI TRONG BÀI HỌC
Câu 1. [CTST – SGK] Trong cuộc sống, chúng ta thường gặp những biến đổi hoá học như trái cây xanh (vị chát) chuyển thành trái cây chín (vị ngọt), đốt gas để nấu chín thực phẩm, thức ăn để lâu bị ôi thiu, … Những biến đổi này đều xảy ra phản ứng hoá học. Phản ứng hoá học là gì? Dấu hiệu nào chứng tỏ có phản ứng hoá học xảy ra
Hướng dẫn giải:
– Khi một chất bị biến đổi hoá học sẽ có chất mới được tạo thành, quá trình này được gọi là phản ứng hoá học.
– Dấu hiệu chứng tỏ có phản ứng hoá học xảy ra: xuất hiện chất khí, chất kết tủa; thay đổi màu sắc, mùi; phát sáng, giải phóng hoặc hấp thụ nhiệt năng, …
Câu 2. [CTST – SGK] Hỗn hợp sau khi đun nóng còn tính chất của iron nữa không? Vì sao?

Hướng dẫn giải:
Hỗn hợp sau khi đun nóng không còn tính chất của iron do hỗn hợp này không bị nam châm hút.
Câu 3. [CTST – SGK] Xác định chất tham gia và chất mới tạo thành của phản ứng hoá học xảy ra trong thí nghiệm.
Hướng dẫn giải:
– Chất tham gia: sắt, lưu huỳnh;
– Chất mới tạo thành: iron(II) sulfide (FeS).
Câu 4. [CTST – SGK] Để tổng hợp ammonia (nguyên liệu sản xuất phân đạm), người ta cho khí hydrogen phản ứng với khí nitrogen ở nhiệt độ thích hợp và áp suất cao. Xác định chất đầu và sản phẩm.
Hướng dẫn giải:
– Chất đầu: hydrogen; nitrogen.
– Sản phẩm: ammonia.
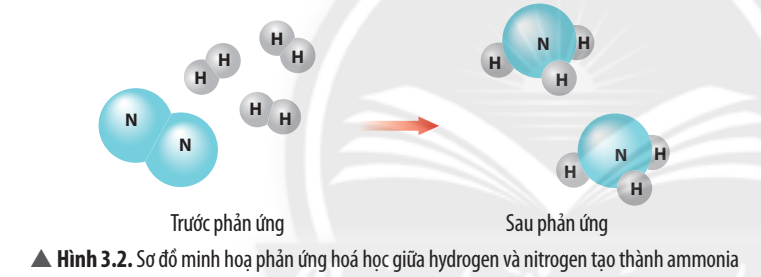
Câu 5. [CTST – SGK] Quan sát Hình 3.2, hãy cho biết:
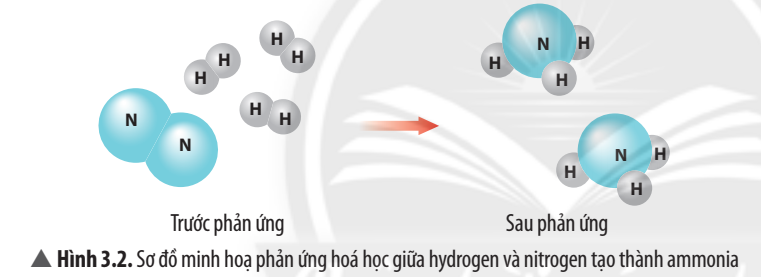
a) trước và sau phản ứng những nguyên tử nào liên kết với nhau.
b) số nguyên tử H cũng như số nguyên tử N có thay đổi không.
Hướng dẫn giải:
a) Trước phản ứng H liên kết với H; N liên kết với N. Sau phản ứng N liên kết với H.
b) Số nguyên tử H cũng như số nguyên tử N không thay đổi.
Câu 6. [CTST – SGK] Hãy chỉ ra các dấu hiệu chứng tỏ đã có phản ứng hoá học xảy ra trong các hiện tượng ở các hình từ 3.3 đến 3.6.
 |
 |
 |
 |
| (3.3) | (3.4) | (3.5) | (3.6) |
Hướng dẫn giải:
Dấu hiệu chứng tỏ đã có phản ứng hoá học xảy ra:
– Hình 3.3: có sự phát sáng và giải phóng nhiệt năng;
– Hình 3.4: đường chuyển từ màu trắng sang màu nâu rồi màu đen;
– Hình 3.5: xuất hiện bọt khí.
– Hình 3.6: có chất kết tủa tạo thành sau phản ứng.
Câu 7. [CTST – SGK] Hãy chỉ ra dấu hiệu của phản ứng hoá học trong các trường hợp dưới đây:
a) Đinh sắt để lâu trong không khí sẽ xuất hiện lớp gỉ sét màu nâu bám bên ngoài đinh sắt.
b) Dùng củi để nhóm lửa để sưởi ấm.
Hướng dẫn giải:
Dấu hiệu của phản ứng hoá học xảy ra:
a) Xuất hiện lớp gỉ sét màu nâu bám bên ngoài đinh sắt.
b) Có sự phát sáng và giải phóng nhiệt năng.
Câu 8. [CTST – SGK] Hãy chỉ ra điểm giống và khác nhau cơ bản giữa phản ứng toả nhiệt và phản ứng thu nhiệt.
Hướng dẫn giải:
– Giống nhau: Đều có sự thay đổi năng lượng.
– Khác nhau:
+ Phản ứng toả nhiệt: giải phóng nhiệt năng ra môi trường.
+ Phản ứng thu nhiệt: nhận năng lượng từ môi trường xung quanh.
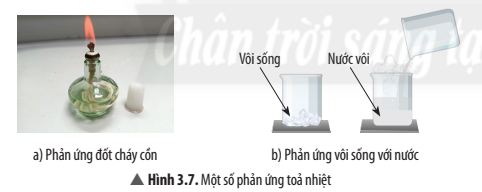
Câu 9. [CTST – SGK] Quan sát Hình 3.7, hãy cho biết hiện tượng xảy ra khi đốt cháy cồn, cho nước vào vôi sống.
Hướng dẫn giải:
– Đốt cháy cồn: cồn cháy, toả nhiều nhiệt;
– Cho vôi sống vào nước: nước sôi, toả nhiều nhiệt.
Câu 10. [CTST – SGK] Hãy cho biết phản ứng toả nhiệt hay thu nhiệt trong mỗi trường hợp sau:
a) Ngọn nến đang cháy.
b) Hoà tan viên vitamin C sủi vào nước.
Hướng dẫn giải:
a) Ngọn nến đang cháy: phản ứng toả nhiệt;
b) Hoà tan viên vitamin C sủi vào nước: phản ứng thu nhiệt.
Câu 11. [CTST – SGK] Vì sao người ta sử dụng xăng, dầu, than làm nhiên liệu trong đời sống và sản xuất?

Hướng dẫn giải:
Do xăng, dầu, than dễ cháy và khi cháy toả nhiều nhiệt nên được sử dụng làm nhiên liệu trong đời sống và sản xuất.
Câu 12. [CTST – SGK] Các phương tiện giao thông cơ giới (xe máy, ô tô, …) khi chạy bằng nhiên liệu xăng, dầu thường làm nóng máy trong quá trình vận hành. Nguồn nhiệt này chủ yếu tạo ra từ đâu?
Hướng dẫn giải:
Nguồn nhiệt này chủ yếu được tạo ra từ quá trình đốt cháy nhiên liệu.
C. CÂU HỎI CUỐI BÀI HỌC
KHÔNG CÓ
D. TỰ LUẬN
Câu 1. Các quá trình sau đây là tỏa nhiệt hay thu nhiệt?
a) Sulfuric acid đặc khi thêm vào nước làm cho nước nóng lên.
b) Quá trình chạy của con người.
c) Sự tiêu hóa thức ăn.
d) Nước hóa rắn.
Hướng dẫn giải:
a) Sulfuric acid đặc khi thêm vào nước làm cho nước nóng lên là quá trình tỏa nhiệt.
b) Quá trình chạy của con người là quá trình tỏa nhiệt.
c) Sự tiêu hóa thức ăn là quá trình thu nhiệt.
d) Nước hóa rắn là quá trình tỏa nhiệt.
Câu 2. Chỉ ra dấu hiệu cho thấy đã có phản ứng hóa học xảy ra trong các quá trình sau. Hãy viết phương trình chữ của phản ứng và xác định chất phản ứng, sản phẩm của các phản ứng.
(a) Khi đốt nến (làm bằng parafin), nến cháy trong không khí (tác dụng với oxygen) tạo ra khí carbon dioxide và hơi nước.
(b) Bỏ quả trứng vào dung dịch hydrochloric acid thấy sủi bọt khí ở vỏ. Biết rằng hydrochloric acid đã tác dụng với calcium carbonate (chất có trong vỏ trứng) tạo ra calcium chloride, nước và khí carbon dioxide
(c) Khi đốt than, than cháy trong không khí (tác dụng với oxygen) tạo ra khí carbon dioxide.
(d) Nước vôi (calcium hydroxide) được quét lên tường một thời gian sau đó sẽ khô và hóa rắn (chất rắn là calcium carbonate). Biết rằng khí carbon dioxide đã tham gia phản ứng và sản phẩm còn có nước.
Hướng dẫn giải:
(a) Hiện tượng tạo thành chất mới là khí carbon dioxide và hơi nước.
Parafin + Oxygen $\xrightarrow{{{t^ \circ }}}$ Khí carbon dioxide + Nước.
Chất đầu: Parafin; oxygen
Sản phẩm: Khí carbon dioxide; nước.
(b) Hiện tượng tạo thành chất mới là calcium chloride, nước và khí carbon dioxide.
Calcium carbonate + Hydrochloric acid → Calcium chloride + Nước + Khí carbon dioxide
Chất đầu: Calcium carbonate; hydrochloric acid
Sản phẩm: Calcium chloride, nước và khí carbon dioxide.
(c) Hiện tượng tạo thành chất mới là khí carbon dioxide.
Than + Oxygen $\xrightarrow{{{t^ \circ }}}$ Khí carbon dioxide
Chất đầu: Than; Oxygen
Sản phẩm: Khí carbon dioxide.
(d) Hiện tượng tạo thành chất mới là calcium carbonate.
Calcium hydroxide + Khí carbon dioxide → Calcium carbonate + Nước
Chất đầu: Calcium hydroxide; khí carbon dioxide
Sản phẩm: Calcium carbonate; nước.
 Câu 3. Để sản xuất sulfuric acid (H2SO4) là một hóa chất quan trọng trong nhiều ngành sản xuất người ta dùng nguyên liệu là quặng pyrite (FeS2). Ban đầu người ta đem nghiền nhỏ quặng pyrite rồi nung ở nhiệt độ cao thu được iron (III) oxide (Fe2O3) và sulfur dioxide (SO2). Sau đó oxygen hóa sulfur dioxide bằng oxygen với xúc tác thích hợp ở 450 ℃ thu được sulfur trioxide (SO3). Cuối cùng cho sulfur trioxide vào nước người ta thu được sulfuric acid.
Câu 3. Để sản xuất sulfuric acid (H2SO4) là một hóa chất quan trọng trong nhiều ngành sản xuất người ta dùng nguyên liệu là quặng pyrite (FeS2). Ban đầu người ta đem nghiền nhỏ quặng pyrite rồi nung ở nhiệt độ cao thu được iron (III) oxide (Fe2O3) và sulfur dioxide (SO2). Sau đó oxygen hóa sulfur dioxide bằng oxygen với xúc tác thích hợp ở 450 ℃ thu được sulfur trioxide (SO3). Cuối cùng cho sulfur trioxide vào nước người ta thu được sulfuric acid.
(a) Hãy cho biết trong quá trình trên giai đoạn nào xảy ra biến đổi vật lí? Giai đoạn nào xảy ra biến đổi hóa học? Giải thích.
(b) Viết phương trình chữ của phản ứng hóa học.
Hướng dẫn giải:
(a) – Nghiền nhỏ quặng pyrite: Biến đổi vật lí vì quặng thay đổi về hình dạng.
– Nung quặng ở nhiệt độ cao: Biến đổi hóa học vì hiện tượng tạo ra chất mới là iron (III) oxide (Fe2O3) và sulfur dioxide (SO2).
– Oxi hóa sulfur dioxide bằng oxygen: Biến đổi hóa học vì tạo ra chất mới là sulfur trioxide (SO3).
– Cho sulfur trioxide vào nước: Biến đổi hóa học vì tạo ra chất mới là sulfuric acid.
(b) Pyrite + Oxygen $\xrightarrow{{{t^ \circ }}}$ Iron (III) oxide + Sulfur dioxide
Sulfur dioxide + Oxygen $\xrightarrow{{{t^ \circ }}}$ Sulfur trioxide
Sulfur trioxide + Nước → Sulfuric acid.
Câu 4. Chỉ ra dấu hiệu cho thấy đã có phản ứng hóa học xảy ra trong các quá trình sau. Hãy viết phương trình chữ của phản ứng và xác định chất phản ứng, sản phẩm của các phản ứng.
(a) Hòa tan bột copper (II) oxide vào dung dịch hydrochloric acid không màu thu được dung dịch copper (II) chloride có màu xanh. Biết rằng sản phẩm của phản ứng còn có nước.
(b) Thả mảnh nhôm (aluminium) vào dung dịch sulfuric acid thu được dung dịch aluminium sulfate và thấy có sủi bọt khí (hydrogen).
(c) Nhỏ vài giọt barium chloride vào dung dịch sulfuric acid thấy xuất hiện chất kết tủa màu trắng (barium sulfate). Biết rằng sản phẩm của phản ứng còn có hydrochloric acid.
Hướng dẫn giải:
(a) Sản phẩm tạo thành chất mới là dung dịch copper (II) chloride có màu xanh.
Copper (II) oxide + Hydrochloric acid → Copper (II) chloride + Nước
Chất đầu: Copper (II) oxide; hydrochloric acid
Sản phẩm: Copper (II) chloride; nước
(b) Sản phẩm tạo thành chất mới là dung dịch aluminium sulfate và có sủi bọt khí (hydrogen).
Nhôm (aluminium) + Sulfuric acid → Aluminium sulfate + Hydrogen
Chất đầu: Nhôm; Sulfuric acid
Sản phẩm: aluminium sulfate; hydrogen
(c) Sản phẩm tạo thành chất mới là chất kết tủa màu trắng (barium sulfate).
Barium chloride + Sulfuric acid → Barium sulfate + Hydrochloric acid
Chất phản ứng: Barium chloride; sulfuric acid
Sản phẩm: Barium sulfate ; hydrochloric acid
Câu 5. Biết rằng trong nước bọt có men amylase làm chất xúc tác cho phản ứng của starch với nước chuyển thành maltose (đường mạch nha) và một ít men mantaza làm chất xúc tác cho phản ứng của maltose với nước chuyển thành glucose.
Khi nhai cơm (trong cơm có starch) có thể xảy ra hai phản ứng hóa học trên. Hãy ghi lại phương trình chữ của hai phản ứng và giải thích vì sao khi nhai kĩ cơm ta thấy có vị hơi ngọt. 
Hướng dẫn giải:
Starch $\xrightarrow{{men{\text{ amilaza}}}}$Maltose $\xrightarrow{{men{\text{ mantaza}}}}$ Glucose
Khi nhai kỹ cơm ta thấy có vị hơi ngọt vì nước bọt có men amylase và men mantaza làm chất xúc tác cho phản ứng của starch với nước chuyển thành maltose (đường mạch nha) và glucose.
E. BÀI TẬP TRẮC NGHIỆM
MỨC ĐỘ 1: BIẾT (7 câu biết)
Câu 1. Phản ứng hóa học là
A. quá trình kết hợp các đơn chất thành hợp chất.
B. quá trình biến đổi chất này thành chất khác.
C. sự trao đổi của 2 hay nhiều chất ban đầu để tạo chất mới.
D. là quá trình phân hủy chất ban đầu thành nhiều chất.
Câu 2. Phản ứng tỏa nhiệt là phản ứng trong đó
A. hỗn hợp phản ứng truyền nhiệt cho môi trường.
B. chất phản ứng truyền nhiệt cho sản phẩm.
C. chất phản ứng thu nhiệt từ môi trường
D. các chất sản phẩm thu nhiệt từ môi trường.
Câu 3. Phản ứng thu nhiệt là phản ứng trong đó
A. các chất sản phẩm truyền nhiệt cho môi trường.
B. các chất sản phẩm nhận nhiệt từ các chất phản ứng.
C. các chất phản ứng truyền nhiệt cho môi trường.
D. hỗn hợp phản ứng nhận nhiệt từ môi trường.
 Câu 4. Hiện tượng nào là hiện tượng hoá học trong các hiện tượng thiên nhiên sau đây?
Câu 4. Hiện tượng nào là hiện tượng hoá học trong các hiện tượng thiên nhiên sau đây?
A. Sáng sớm, khi mặt trời mọc sương mù tan dần.
B. Hơi nước trong các đám mây ngưng tụ và rơi xuống tạo ra mưa.
C. Nạn cháy rừng tạo khói đen dày đặc gây ô nhiễm môi trường.
D. Khi mưa giông thường có sấm sét.
Câu 5. Sản phẩm của phản ứng: natri (sodium) + oxygen → sodium oxide là
A. natri (sodium).
B. oxygen.
C. sodium oxide.
D. natri (sodium) và oxygen.
Câu 6. Sản phẩm của phản ứng: Sắt (iron) + hydrochloric acid → iron (II) chloride + hydrogen là
A. sắt (iron).
B. hydrochloric acid.
C. iron (II) chloride.
D. iron (II) chloride và hydrogen.
Câu 7. Cho phản ứng: iron (II) hydroxide + oxygen + nước → iron (III) hydroxide. Số chất phản ứng trong phản ứng trên là
A. 3.
B. 2.
C. 1.
D. 4.
ĐÁP ÁN
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| B | A | D | C | C | D | B |
MỨC ĐỘ 2 : HIỂU (5 câu )
Câu 1. Dấu hiệu nào sau đây chứng tỏ đã có phản ứng hoá học xảy ra?
A. Thay đổi màu sắc.
B. Thay đổi trạng thái (có chất khí sinh ra, có xuất hiện kết tủa).
C. Tỏa nhiệt và phát sáng.
D. Cả A, B, C
Câu 2. Phát biểu nào sau đây đúng?
A. Trong phản ứng hoá học, các nguyên tử bị phá vỡ.
B. Trong phản ứng hoá học, liên kết trong các phân tử bị phá vỡ.
 C. Trong phản ứng hoá học, liên kết trong các phân tử không bị phá vỡ.
C. Trong phản ứng hoá học, liên kết trong các phân tử không bị phá vỡ.
D. Trong phản ứng hoá học các phân tử được bảo toàn.
Câu 3. Phản ứng nào sau đây là phản ứng toả nhiệt?
A. Phản ứng nung đá vôi CaCO3.
B. Phản ứng đốt cháy khí gas.
C. Phản ứng hòa tan viên C sủi vào nước.
D. Phản ứng phân hủy đường.
Câu 4. Những loại phản ứng nào sau đây cần phải cung cấp năng lượng trong quá trình phản ứng?
A. Phản ứng đốt cháy cồn.
B. Phản ứng quang hợp.
C. Phản ứng đốt cháy xăng.
D. Phản ứng đốt cháy que diêm.
Câu 5. Sự biến đổi nào sau đây không phải là một biến đổi hóa học?
A. Hơi nến cháy trong không khí tạo thành khí carbonic và hơi nước.
B. Hòa tan muối ăn vào nước tạo thành dung dịch muối.
C. Sắt (iron) cháy trong lưu huỳnh (sulfur) tạo thành muối iron (II) sufide.
D. Khí hydrogen cháy trong oxygen tạo thành nước.
ĐÁP ÁN
| 1 | 2 | 3 | 4 | 5 |
| D | B | B | B | B |
MỨC ĐỘ 3: VẬN DỤNG (GIẢI CHI TIẾT) 3 câu
Câu 1. Cho các quá trình sau:
(1) Về mùa hè thức ăn thường bị ôi thiu.
(2) Đun đường, đường ngả màu nâu rồi chuyển thành màu đen.
(3) Thổi quả bóng bay căng đến phát nổ.
(4) Cháy rừng gây ô nhiễm lớn cho môi trường.
(5) Nhiệt độ trái đất nóng lên làm băng ở hai cực trái đất tan dần.
Những quá trình xảy ra biến đổi hóa học là
A. (1), (2), (3), (4).
B. (1), (2), (4), (5).
C. (1), (2), (4).
D. (1), (4), (5).
 Câu 2. Cho các quá trình sau:
Câu 2. Cho các quá trình sau:
(1) Đinh sắt (iron) để trong không khí bị gỉ.
(2) Sự quang hợp của cây xanh.
(3) Cồn để trong lọ không kín bị bay hơi.
(4) Tách khí oxygen từ không khí.
(5) Rượu để lâu trong không khí thường bị chua.
Số quá trình xảy ra biến đổi hóa học là
A. 4.
B. 2.
C. 3.
D. 1.
Câu 3. Cho một số nhận định sau:
(a) Biến đổi hóa học là sự biến đổi chất có sinh ra chất mới.
(b) Trong phản ứng hóa học, tính chất của các chất vẫn giữ nguyên.
(c) Trong phản ứng hóa học số nguyên tử của mỗi nguyên tố giữ nguyên.
(d) Phản ứng tỏa nhiệt là phản ứng giải phóng năng lượng dưới dạng nhiệt ra môi trường.
(e) Phản ứng hóa học chỉ xảy ra được khi có xúc tác hoặc đun nóng.
Số nhận định sai là:
A. 1.
B. 2.
C. 3
D. 4.
ĐÁP ÁN
| 1 | 2 | 3 |
| C | C | B |