Bài tập trắc nghiệm đơn chất nitrogen Hóa 11 có đáp án được soạn dưới dạng file word gồm 18 trang. Các bạn xem và tải về ở dưới.
Trắc Nghiệm Đơn Chất Nitrogen
Câu 1. Khí nitrogen chiếm tỉ lệ bao nhiêu trong thể tích không khí?
A. $76{\text{% }}$.
B. $77{\text{% }}$.
C. $78{\text{% }}$.
D. $79{\text{% }}$.
Câu 2. Hợp chất hữu cơ nào sau đây không có chứa nitrogen?
A. Amino acid
B. Chlorophyll
C. Nucleic acid
D. Glucose
Câu 3. Ứng dụng nào sau đây không phải của nitrogen ?
A. Làm môi trường trơ trong một số ngành công nghiệp.
B. Bảo quản máu và các mẫu vật sinh học.
C. Sản xuất nitric acid.
D. Sản xuất phân lân.
Câu 4. Đâu không phải là ứng dụng của nitrogen?
A. Bảo quản thực phẩm.
B. Bảo quản mẫu vật.
C. Trộn lẫn, pha loãng xăng.
D. Thay thế khí trơ trong hóa học.
Câu 5. Trong khí quyển nitrogen tồn tại chủ yếu ở dạng?
A. Đơn chất
B. Hợp chất vô cơ
C. Hợp chất hữu cơ
D. Ion
Câu 6. Tính kém hoạt động của đơn chất nitrogen ở nhiệt độ thấp là do?
A. Đôi điện tử tự do còn lại trên nguyên tử ${\text{N}}$.
B. Nitrogen bị thụ động hóa ở nhiệt độ thấp.
C. Liên kết ba giữa hai nguyên tử ${\text{N}}$ có năng lượng liên kết lớn.
D. Ở nhiệt độ thấp, nitrogen hóa lỏng nên không thể tham gia phản ứng hóa học.
Câu 7. ${\text{N}}{{\text{O}}_3}{^ – }$là dạng tồn chủ yếu của nitrogen ở đâu?
A. Đất
B. Cơ thể
C. Khí quyển
D. Quặng mỏ
Câu 8. Khi có sấm sét, nitrogen tác dụng với oxygen tạo ra?
A. ${\text{N}}{{\text{O}}_2}$
B. ${\text{HN}}{{\text{O}}_3}$.
C. ${{\text{N}}_2}{\text{O}}$.
D. NO.
Câu 9. Nitrogen được sản xuất chủ yếu ở dạng?
A. Khí
B. Lỏng
C. Bột mịn
D. Tinh thể
Câu 10. Trong phản ứng nào sau đây, nitrogen thể hiện tính khử ?
A. ${{\text{N}}_2} + 3{{\text{H}}_2} \leftrightharpoons 2{\text{N}}{{\text{H}}_3}$
B. ${{\text{N}}_2} + 6{\text{Li}} \to 2{\text{L}}{{\text{i}}_3}{\text{N}}$
C. ${{\text{N}}_2} + {{\text{O}}_2} \leftrightharpoons 2{\text{NO}}$
D. ${{\text{N}}_2} + 3{\text{Mg}} \to {\text{M}}{{\text{g}}_3}{\text{}}{{\text{N}}_2}$
Câu 11. Khí ${{\text{N}}_2}$ tác dụng với dãy chất nào sau đây:
A. ${\text{C}}{{\text{l}}_2}$ và ${{\text{O}}_2}$
B. ${{\text{H}}_2}$ và ${\text{C}}{{\text{l}}_2}$
C. ${{\text{H}}_2}$ và ${\text{C}}{{\text{O}}_2}$
D. ${{\text{H}}_2}$ và ${{\text{O}}_2}$
Câu 12. Vì sao nitrogen lỏng có thể được sử dụng để làm lạnh nhanh?
A. Vì nitrogen lỏng phá hủy cấu trúc vật chất, sinh ra chất làm lạnh.
B. Vì nitrogen lỏng làm chết vi khuẩn phân hủy vật chất.
C. Vì nitrogen hóa lỏng ở nhiệt độ rất thấp.
D. Vì nitrogen có tính oxy hóa vô cùng mạnh.
Câu 13. Ở $ – {200^ \circ }{\text{C}}$, nitrogen tồn tại ở dạng nào?
A. Lỏng
B. Khí
C. Rắn
D. Bán rắn
Câu 14. Khi có tia lửa điện hoặc ở nhiệt độ cao, nitrogen tác dụng trực tiếp với oxygen tạo ra hợp chất $X$. Công thức của ${\text{X}}$ là:
A. ${{\text{N}}_2}{\text{O}}$.
B. ${\text{N}}{{\text{O}}_2}$.
C. NO.
D. ${{\text{N}}_2}{{\text{O}}_5}$.
Câu 15. Nitrogen thể hiện tính khử trong phản ứng với chất nào sau đây ?
A. ${{\text{H}}_2}$.
B. ${{\text{O}}_2}$.
C. ${\text{Mg}}$.
D. ${\text{Al}}$.
Câu 16. Nguồn cung cấp đạm cho đất là ion nào sau đây?
A. ${\text{N}}{{\text{O}}_3}{^ – }$
B. ${\text{N}}{{\text{O}}_2}{^ – }$
C. ${\text{N}}{{\text{H}}_4}{^ + }$
D. ${{\text{N}}^{3 – }}$
Câu 17. Nitrogen lỏng có thể gây?
A. Bỏng lạnh
B. Đóng băng
C. Ăn mòn
D. Xuất huyết
Câu 18. Trong không khí chứa chủ yếu hai khí nào sau đây?
A. ${{\text{N}}_2},{\text{C}}{{\text{O}}_2}$
B. ${{\text{N}}_2},{{\text{O}}_2}$
C. ${\text{C}}{{\text{O}}_2},{{\text{O}}_2}$
D. ${{\text{O}}_2},{\text{N}}{{\text{H}}_3}$
Câu 19. Hình bên dưới mô tả thí nghiệm khi cho một ngọn nến đang cháy vào bình khí nitrogen, giải thích nào sau đây là đúng?
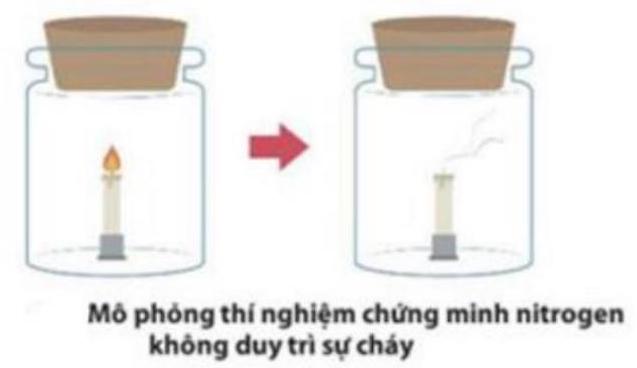
A. Ngọn nến cháy, do nitrogen duy trì sự cháy
B. Ngọn nến tắt do nitrogen không duy trì sự cháy
C. Ngọn nến tắt do thiếu carbon dioxide không duy trì sự cháy
D. Ngọn nến cháy, do được cách ly với oxygen.
Câu 20. Trong phòng thí nghiệm, để điều chế một lượng nhỏ khí ${{\text{N}}_2}$, người ta đun nóng dung dịch muối $X$ bão hòa. Muối $X$ là:
A. ${\text{N}}{{\text{H}}_4}{\text{N}}{{\text{O}}_2}$
B. ${\text{NaN}}{{\text{O}}_3}$
C. ${\text{N}}{{\text{H}}_4}{\text{Cl}}$
D. ${\text{N}}{{\text{H}}_4}{\text{N}}{{\text{O}}_3}$
Câu 21. Khí không màu hóa nâu trong không khí là
A. ${{\text{N}}_2}{\text{O}}$.
B. NO.
C. ${\text{N}}{{\text{H}}_3}$.
D. ${\text{N}}{{\text{O}}_2}$.
Câu 22. Nitrogen là chất khí phổ biến trong khí quyển trái đất và được sử dụng chủ yếu để sản xuất ammonia. Số oxy hóa của nguyên tố ${\text{N}}$ trong phân tử ${{\text{N}}_2}$ là:
A. 0
B. 1
C. 2
D. 3
Câu 23. Kim loại nào sau đây có thể tác dụng với khí ${{\text{N}}_2}$ ở nhiệt độ thường.
A. ${\text{Li}}$
B. ${\text{Cs}}$
C. K
D. ${\text{Ca}}$
Câu 24. Ở điều kiện thường, không tồn tại hỗn hợp khí
A. ${{\text{N}}_2},{{\text{O}}_2}$
B. ${\text{NO}},{{\text{O}}_2}$
C. ${{\text{N}}_2},{\text{C}}{{\text{O}}_2}$
D. ${{\text{N}}_2},{{\text{H}}_2}$
Câu 25. Người ta sản xuất khi nitrogen trong công nghiệp bằng cách nào sau đây?
A. Chưng cất phân đoạn không khí lỏng.
B. Nhiệt phân dung dịch ${\text{N}}{{\text{H}}_4}{\text{N}}{{\text{O}}_2}$ bão hoà.
C. Dùng phospho để đốt cháy hết oxygen không khí.
D. Cho không khí đi qua bột đồng nung nóng.
Câu 26. Hiệu suất của phản ứng giữa ${{\text{N}}_2}$ và ${{\text{H}}_2}$ tạo thành ${\text{N}}{{\text{H}}_3}$ tăng nếu:
A. Giảm áp suất, tăng nhiệt độ.
B. Giảm áp suất, giảm nhiệt độ.
C. Tăng áp suất, tăng nhiệt độ.
D. Tăng áp suất, giảm nhiệt độ.
Câu 27. Ở nhiệt độ thường, nitrogen khá trơ về mặt hoạt động là do
A. Nitrogen có bán kính nguyên tử nhỏ.
B. Nitrogen có độ âm điện lớn nhất trong nhóm.
C. Phân tử nitrogen có liên kết ba khá bền.
D. Phân tử nitrogen không phân cực.
Câu 28. Khi có tia lửa điện hoặc nhiệt độ cao. Nitrogen tác dụng trực tiếp với oxygen tạo ra hợp chất $X$. X tiếp tục tác dụng với oxygen trong không khí tạo thành hợp chất Y. Công thức của ${\text{X}},{\text{Y}}$ lần lượt là:
A. ${{\text{N}}_2}{\text{O}},{\text{NO}}$.
B. ${\text{N}}{{\text{O}}_2},{\text{}}{{\text{N}}_2}{{\text{O}}_5}$.
C. ${\text{NO}},{\text{N}}{{\text{O}}_2}$.
D. ${{\text{N}}_2}{{\text{O}}_5},{\text{HN}}{{\text{O}}_3}$.
Câu 29. Để loại bỏ các khí ${\text{HCl}},{\text{C}}{{\text{l}}_2},{\text{C}}{{\text{O}}_2}$ và ${\text{S}}{{\text{O}}_2}$ có lẫn trong khí ${{\text{N}}_2}$ người ta sử dụng lượng dư dung dịch
A. ${\text{AgN}}{{\text{O}}_3}$.
B. ${\text{Ca}}{({\text{OH}})_2}$.
C. ${{\text{H}}_2}{\text{S}}{{\text{O}}_4}$.
D. ${\text{CuC}}{{\text{l}}_2}$.
Câu 30. Nitrogen có số oxy hóa âm trong hợp chất với nguyên tố nào sau đây ?
A. ${\text{H}}$.
B. ${\text{O}}$.
C. ${\text{Cl}}$.
D. F.
Câu 31. Vận dụng tính chất nào của khí nitrogen mà người ta ứng dụng nó để làm các hệ thống chữa cháy?
A. Tính trơ
B. Tính khử
C. Tính oxy hóa
D. Tính chất khí
Câu 32. Trong cấu tạo của bình bảo quản mẫu vật bằng nitrogen lỏng thường có khoang chân không với mục đích là:
A. Tạo môi trường trơ.
B. Hạn chế vi khuẩn xâm nhập.
C. Tạo áp suất trong bình.
D. Cách nhiệt với môi trường.
Câu 33. Aluminium nitride là một vật liệu thú vị và là một trong những vật liệu tốt nhất để sử dụng nếu cần độ dẫn nhiệt cao. Khi kết hợp với các đặc tính cách điện tuyệt vời của nó, nhôm nitride là vật liệu tản nhiệt lý tưởng cho nhiều ứng dụng điện và điện tử. Trong số các ứng dụng của nhôm nitride là quang điện tử, các lớp điện môi trong phương tiện lưu trữ quang học, chất nền điện tử, chất mang chip nơi dẫn nhiệt cao là điều cần thiết, ứng dụng quân sự. Công thức hoá học của aluminium nitride là :
A. ${\text{A}}{{\text{l}}_3}{\text{N}}$
B. AlN
C. ${\text{Al}}{{\text{N}}_3}$
D. ${\text{A}}{{\text{l}}_2}{\text{}}{{\text{N}}_3}$
Câu 34. Chất diệp lục là hợp chất hữu cơ của nitrogen với tên gọi là:
A. Chloroform
B. Dichloromethane
C. Butaphosphane
D. Chlorophyll
Câu 35. Hiệu suất của phản ứng giữa ${{\text{N}}_2}$ và ${{\text{H}}_2}$ tạo thành ${\text{N}}{{\text{H}}_3}$ giảm nếu:
A. Giảm áp suất, tăng nhiệt độ.
B. Giảm áp suất, giảm nhiệt độ.
C. Tăng áp suất, tăng nhiệt độ.
D. Tăng áp suất, giảm nhiệt độ.
Câu 36. Trong phòng thí nghiệm người ta điều chế ${{\text{N}}_2}$ bằng cách đun hỗn hợp chất nào với ${\text{N}}{{\text{H}}_4}{\text{Cl}}$ :
A. ${\text{NaN}}{{\text{O}}_3}$
B. ${\text{NaN}}{{\text{O}}_2}$
C. ${\text{M}}{{\text{g}}_3}{\text{}}{{\text{N}}_2}$
D. ${\text{HN}}{{\text{O}}_3}$
Câu 37. Nhiệt phân chất nào sau đây thu được khí nitrogen?
A. ${\text{N}}{{\text{H}}_4}{\text{N}}{{\text{O}}_3}$
B. ${\text{N}}{{\text{H}}_4}{\text{Cl}}$
C. ${\text{N}}{{\text{H}}_4}{\text{N}}{{\text{O}}_2}$
D. ${\text{N}}{{\text{H}}_4}{\text{N}}{{\text{O}}_3}$
Câu 38. Khí ${{\text{N}}_2}$ không tác dụng với chất nào sau đây?
A. ${\text{Li}}$
B. ${{\text{H}}_2}$
C. ${{\text{O}}_2}$
D. ${\text{N}}{{\text{O}}_2}$
Câu 39. Xúc tác cho phản ứng giữa nitrogen và hydrogen là?
A. Bột ${\text{Cu}}$
B. Bột Zn
C. Bột Fe
D. Bột ${\text{Al}}$
Câu 40. Ở mức nhiệt độ nào, phản ứng giữa nitrogen và hydrogen không diễn ra?
A. ${1000^ \circ }{\text{C}}$
B. ${3000^ \circ }{\text{C}}$
C. ${5000^ \circ }{\text{C}}$
D. ${10000^ \circ }{\text{C}}$
Câu 41. Quan sát hình bên dưới và từ dữ kiện năng lượng liên kết trong phân tử ${{\text{N}}_2}$, dự đoán về độ bền phân tử và khả năng phản ứng của nitrogen ở nhiệt độ thường.
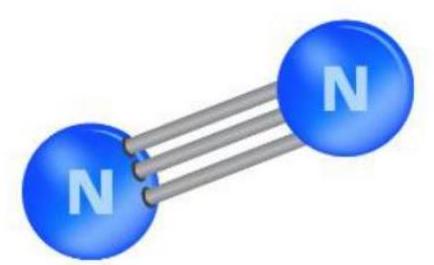
${E_b}\left( {N \equiv N} \right) = 945{\text{kJ}}/{\text{mol}}$
A. Kém bền và hoạt động hóa học mạnh ở nhiệt độ thường.
B. Bền và trơ về mặt hóa học ở nhiệt độ thường.
C. Bền và hoạt động hóa học mạnh ở nhiệt độ thường.
D. Kém bền và trơ về mặt hóa học mạnh ở nhiệt độ thường
Câu 42. Trong các hợp chất hoá học sau hợp chất nào nitrogen có số oxygen hoá cực tiểu ?
A. ${\left( {{\text{N}}{{\text{H}}_4}} \right)_2}{\text{S}}{{\text{O}}_4}$
B. ${{\text{N}}_2}$
C. ${\text{N}}{{\text{O}}_2}$
D. ${\text{HN}}{{\text{O}}_2}$
Câu 43. Tìm phát biểu sai:
A. Nitrogen là chất khí không màu, không mùi, không vị.
B. Nitrogen nhẹ hơn không khí
C. Nitrogen tan rất ít trong nước
D. Nitrogen duy trì sự cháy và sự hô hấp
Câu 44. Cho các phản ứng sau :
(1) ${{\text{N}}_2} + {{\text{O}}_2} \leftrightharpoons 2{\text{NO}}$
(2) ${{\text{N}}_2} + 3{{\text{H}}_2} \leftrightharpoons 2{\text{N}}{{\text{H}}_3}$
Trong hai phản ứng trên thì nitrogen
A. chỉ thể hiện tính oxi hóa.
B. chỉ thể hiện tính khử.
C. thể hiện cả tính khử và tính oxi hóa.
D. không thể hiện tính khử và tính oxi hóa.
Câu 45. Trong phòng thí nghiệm người ta thu khí nitrogen bằng phương pháp dời nước vì:
A. ${{\text{N}}_2}$ nhẹ hơn không khí.
B. ${{\text{N}}_2}$ rất ít tan trong nước.
C. ${N_2}$ không duy trì sự sống, sự cháy.
D. ${{\text{N}}_2}$ hoá lỏng, hóa rắn ở nhiệt độ rất thấp.
Câu 46. Chỉ ra nội dung sai
A. ${{\text{N}}_2}$ vừa có tính oxi hóa vừa có tính khử
B. Tính oxi hóa là tính chất đặc trưng của nitrogen
C. ${{\text{N}}_2}$ là chất khí không màu, không mùi
D. Ở điều kiện thường, ${{\text{N}}_2}$ tác dụng được với nhiều chất.
Câu 47. ${{\text{N}}_2}$ phản ứng với ${{\text{O}}_2}$ tạo thành ${\text{NO}}$ ở điều kiện nào dưới đây ?
A. Nhiệt độ phản ứng khoảng ${100^ \circ }{\text{C}}$
B. Nhiệt độ phản ứng rất cao khoảng ${3000^ \circ }{\text{C}}$ hoặc có tia lửa điện.
C. Nhiệt độ phản ứng khoảng ${500^ \circ }{\text{C}}$
D. Điều kiện thường, vì nitrogen là phi kim hoạt động mạnh.
Câu 48. Hãy sắp xếp các công thức sau theo thứ tự tăng dần về số oxi hóa của nguyên tố nitrogen. ${{\text{N}}_2}{\text{NO}},{\text{N}}{{\text{H}}_3},{\text{}}{{\text{N}}_2}{\text{O}},{\text{N}}{{\text{H}}_2}{\text{OH}},{\text{HN}}{{\text{O}}_3},{\text{}}{{\text{N}}_2}{{\text{H}}_4},{\text{N}}{{\text{O}}_2},{\text{HN}}{{\text{O}}_2}$
A. ${{\text{N}}_2} < {\text{NO}} < {\text{N}}{{\text{H}}_3} < {{\text{N}}_2}{\text{O}} < {\text{N}}{{\text{H}}_2}{\text{OH}} < {\text{HN}}{{\text{O}}_3} < {{\text{N}}_2}{{\text{H}}_4} < {\text{N}}{{\text{O}}_2} < {\text{HN}}{{\text{O}}_2}$.
B. ${\text{N}}{{\text{H}}_3} < {{\text{N}}_2}{{\text{H}}_4} < {{\text{N}}_2} < {\text{NO}} < {{\text{N}}_2}{\text{O}} < {\text{N}}{{\text{H}}_2}{\text{OH}} < {\text{HN}}{{\text{O}}_3} < {\text{N}}{{\text{O}}_2} < {\text{HN}}{{\text{O}}_2}$
C. ${\text{N}}{{\text{H}}_3} < {{\text{N}}_2}{{\text{H}}_4} < {{\text{N}}_2} < {{\text{N}}_2}{\text{O}} < {\text{NO}} < {\text{N}}{{\text{H}}_2}{\text{OH}} < {\text{HN}}{{\text{O}}_2} < {\text{N}}{{\text{O}}_2} < {\text{HN}}{{\text{O}}_3}$
D. ${\text{N}}{{\text{H}}_3} < {{\text{N}}_2}{{\text{H}}_4} < {\text{N}}{{\text{H}}_2}{\text{OH}} < {{\text{N}}_2} < {{\text{N}}_2}{\text{O}} < {\text{NO}} < {\text{HN}}{{\text{O}}_2} < {\text{N}}{{\text{O}}_2} < {\text{HN}}{{\text{O}}_3}$
Câu 49. Ở trạng thái cơ bản, các nguyên tố nhóm VA có bao nhiêu electron độc thân ?
A. 1
B. 3
C. 4
D. 5
Câu 50. Trong hợp chất hoá học, nitrogen thường có số oxi hoá:
A. $ + 1, + 2, + 3, + 4, – 4$
B. $1,2,3,4,5,6$
C. $ – 3, + 1, + 2, + 3, + 4, + 5$
D. $ + 2, – 2, + 4, + 6$
ĐÁP ÁN
|
1 |
2 | 3 | 4 | 5 |
|
C |
D | D | C | A |
| 6 | 7 | 8 | 9 |
10 |
|
C |
A | D | A | C |
| 11 | 12 | 13 | 14 |
15 |
|
B |
C | A | C | B |
| 16 | 17 | 18 | 19 |
20 |
|
A |
A | B | B | A |
| 21 | 22 | 23 | 24 |
25 |
|
B |
A | A | B | A |
| 26 | 27 | 28 | 29 |
30 |
|
D |
C | C | B | A |
| 31 | 32 | 33 | 34 |
35 |
|
A |
D | B | D | A |
| 36 | 37 | 38 | 39 |
40 |
|
B |
C | D | C | A |
| 41 | 42 | 43 | 44 |
45 |
|
B |
A | D | C | B |
| 46 | 47 | 48 | 49 |
50 |
| D | B | D | B |
C |