Đề cương ôn tập giữa học kỳ 2 Hóa 11 Kết nối tri thức có đáp án được soạn dưới dạng file word và PDF gồm 5 trang. Các bạn xem và tải về ở dưới.
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ Câu 1 đến Câu 18. Mỗi Câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Tên của alkane nào sau đây không đúng?
A. 2 – methylbutane. B. 3 – methyl butane.
C. 2,2 – dimethylbutane. D. 2,3 – dimethylbutane.
Câu 2. Ở điều kiện thường hydrocarbon nào sau đây ở thể lỏng?
A. Ehtane. B. Propane. C. Butane. D. Pentane.
Câu 3. Trong bình gas đun nấu trong sinh hoạt hàng ngày thường chứa các alkane
A. propane và butane B. methane và ethane.
C. ethane và propane D. butane và pentane.
Câu 4. Biện pháp nào dưới đây không giúp giảm ô nhiễm môi trường do các phương tiện giao thông gây ra?
A. Sử dụng các nhiên liệu như xăng, dầu diesel.
B. Sử dụng các loại nhiên liệu sinh học như xăng E5.
C. Sử dụng các loại nhiên liệu cháy sạch.
D. Đưa thêm chất xúc tác vào ống xả động cơ để chuyển hóa các khí thải độc.
Câu 5. Oxi hóa hoàn toàn a mol alkane X cần dùng 2a mol khí oxygen. Tên gọi của alkane X là
A. ethane. B. propane. C. methane. D. isopropane.
Câu 6. Alkyne C4H6 có bao nhiêu đồng phân cho phản ứng thế kim loại (phản ứng với dung dịch chứa AgNO3/NH3)
A. 4. B. 2. C. 1. D. 3.
Câu 7. Chất nào sau đây làm mất màu dung dịch KMnO4 ở điều kiện thường?
A. Benzene. B. Methane. C. Toluene. D. Acetylene.
Câu 8. Khi cho ethyne tác dụng với hydrogen có xúc tác Lindlar (Pd/PbCO3) đun nóng sản phẩm thu được có tên gọi là
A. ethane B. ethyne C. ethene D. methane
Câu 9. Dẫn khí ethene qua dung dịch bromine thấy dung dịch bị mất màu. Sản phẩm tạo ra là
A. CH3-CH2Br B. CH2Br-CH2Br C. CH3-CHBr2 D. CHBr2-CHBr2
Câu 10. Cho sơ đồ phản ứng sau:
HC≡CH + AgNO3/NH3 → X + NH4NO3
X có công thức cấu tạo là ?
A. AgC≡CAg. B. CAg≡CAg.
C. AgC≡AgC. D. CHAg=CHAg
Câu 11. Công thức phân tử nào sau đây có thể là công thức của hợp chất thuộc dãy đồng đẳng của benzene?
A. C8H16. B. C8H14. C. C8H12. D. C8H10.
Câu 12. Cho các hydrocarbon X và Y có công thức cấu tạo sau:
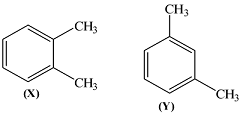
Tên gọi của X và Y lần lượt là
A. p-xylene và m-xylene
B. l,2-dimethylbenzene và l,3-dimethylbenzene.
C. m-xylene và o-xylene.
D. l,3-dimethylbenzene và l,2-dimethylbenzene.
Câu 13. Phân tử benzene có 6 nguyên tử carbon tạo thành hình…………….., tất cả các nguyên tử carbon và hydrogen đều nằm trên một mặt phẳng, có góc liên kết bằng 120o. Cụm từ điền vào khoảng trống là
A. tam giác đều B. lục giác đều C. tròn. D. vuông
Câu 14. Phản ứng của benzene với các chất nào sau đây gọi là phản ứng nitro hóa ?
A. HNO3 đậm đặc. B. HNO3 đặc/H2SO4 đặc.
C. HNO3 loãng/H2SO4 đặc. D. HNO2 đặc/H2SO4 đặc.
Câu 15. Ethyl chloride được dùng làm thuốc xịt có tác dụng giảm đau tạm thời khi chơi thể thao. Công thức phân tử của ethyl chloride là
A. C2H5Cl. B. C2H5F. C. C2H3Cl. D. C2H3F.
Câu 16. Cho phản ứng hóa học sau:
CH3CH2Cl + KOH $\xrightarrow{{{C_2}{H_5}OH,\,{t^0}}}$CH2 = CH2 + KCl + H2O
Phản ứng trên thuộc loại phản ứng nào sau đây?
A. Phản ứng thế. B. Phản ứng cộng.
C. Phản ứng tách. D. Phản ứng oxi hóa – khử.
Câu 17. Tên gọi theo danh pháp thay thế của dẫn xuất halogen có công thức cấu tạo CH3 – CHCl – CH3 là
A. 1-chloropropane. B. 2-chloropropane.
C. 3-chloropropane. D. propyl chloride.
Câu 18. Sản phẩm chính của phản ứng tách HBr của CH3CH(CH3)CHBrCH3 là
A. 3-methyl-but-1-ene. B. 3-methylbut-2-ene.
C. 2-methylbut-1-ene. D. 2-methylbut-2-ene.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ Câu 1 đến Câu 4. Trong mỗi ý a), b), c), d) ở mỗi Câu, thí sinh chọn đúng hoặc sai.
Câu 1. Monochloro hoá propane (có chiếu sáng, ở 25°C), thu được 45% 1-chloropropane và 55% 2-chloropropane; còn monobromine hoá propane (có chiếu sáng và đun nóng đến 127 °C), thu được 4% 1-bromopropane và 96% 2-bromopropane.
a. Bậc của carbon càng cao, phản ứng thế xảy ra càng dễ dàng. Phản ứng thế ở carbon bậc ba dễ hơn ở carbon bậc hai và phản ứng thế ở carbon bậc hai dễ hơn ở carbon bậc một.
b. Sản phẩm 2-chloropropane và 2-bromopropane là sản phẩm phụ còn 1-chloropropane 1-bromopropane là sản phẩm chính.
c. Chlorine tham gia phản ứng thế dễ đàng hơn so với bromine.
d. Phản ứng của bromine yếu, nên bromine chủ yếu lựa chọn phản ứng ở vị trí carbon bậc cao hơn, nơi phản ứng xảy ra dễ dàng hơn.
Câu 2. Thành phần chủ yếu của xăng dầu là hydrocarbon
a. Phải chứa xăng dầu trong các thùng chứa chuyên dụng và bảo quản ở những kho riêng vì chúng dễ gây cháy nổ.
b. Các sự cố tràn dầu trên biển thường gây ra thảm hoạ cho một vùng biển rất rộng vì các hydrocarbon không tan trong nước và nhẹ hơn nước nên loang khắp mặt biển.
c. Khi bị cháy xăng dầu không nên dùng nước để dập đám cháy vì đám cháy sẽ loang nhanh hơn do xăng dầu không tan trong nước và nhẹ hơn nước.
d. Sử dụng xăng pha chì sẽ ít ô nhiễm không khí hơn xăng E5.
Câu 3. Năng lượng liên kết của liên kết C–C (trong phân tử ethane) là 368 kJ mol -1 và năng lượng liên kết của liên kết C=C (trong phân tử ethene) là 636 kJ mol-1.
a. Năng lượng liên kết π trong ethene là 268 kJ mol -1
b. Liên kết π kém bền hơn liên kết σ nên dễ bị bẽ gãy hơn.
c. Ethene dễ tham gia phản ứng hóa học hơn ethane.
d. Ở điều kiện thường ethene tác dụng với hydrogen tạo thành ethane.
Câu 4. Ethene và ethyne là những alkene và alkyene đơn giản nhất. Trung tâm phản ứng của alkene và alkyene là liên kết π trong liên kết đôi C=C và liên kết ba C≡C.
a. Hydrate hóa ethene và ethyne nhận được sản phẩm hữu cơ giống nhau.
b. Liên kết ba C≡C kém bền hơn liên kết đôi C=C.
c. Khi sục hai dòng khí như nhau của ethene và ethyne vào dung dịch KMnO4 thấy enthyne làm nhạt màu dung dịch nhanh hơn ethyne.
d. Góc liên kết HCC trong phân tử ethene và ethyne bằng nhau.
PHẦN III: Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ Câu 1 đến Câu 6.
Câu 1. Tính chỉ số octane của xăng E5, biết xăng E5 chứa 5% ethanol và 95% xăng RON 92 (theo thể tích). (Làm tròn kết quả đến hàng phần mười).
Câu 2. Phân tích thành phần nguyên tố của hợp chất hữu cơ X thu được kết quả %C và %H (theo khối lượng) lần lượt là 84,21% và 15,79%. Phân tử khối của hợp chất X này được xác định thông qua kết quả phổ khối lượng như hình bên dưới với peak ion phân tử có giá trị m/z lớn nhất.
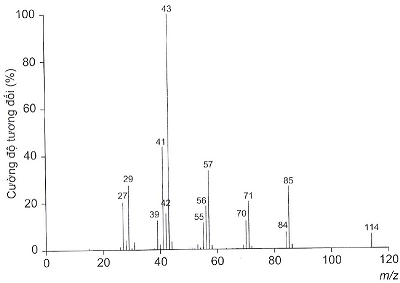
Tổng số nguyên tử trong phân tử của X là bao nhiêu?
Câu 3: Đun sôi 15,7 gam C3H7Cl với hỗn hợp KOH/C2H5OH dư, sau khi loại tạp chất và dẫn khí sinh ra qua dung dịch bromine dư thấy có x gam Br2 tham gia phản ứng. Tính x nếu hiệu suất phản ứng ban đầu là 80%. (Làm tròn kết quả đến hàng phần mười).
Câu 4: Hiện nay PVC được điều chế theo sơ đồ sau:
C2H4 → CH2Cl–CH2Cl → C2H3Cl → PVC.
Nếu hiệu suất toàn bộ quá trình đạt 80% thì lượng C2H4 cần dùng là bao nhiêu tấn để sản xuất 5 tấn PVC? (Làm tròn kết quả đến hàng phần mười).
Câu 5. Propene là nguyên liệu cho sản xuất nhựa polypropylene (PP). PP được sử dụng để sản xuất các sản phẩm ống, màng, dây cách điện, kéo sợi, đồ gia dụng và các sản phẩm tạo hình khác.
Phản ứng tạo thành propene từ propyne:
CH3-C≡CH(g) + H2(g)$\xrightarrow{{{t^0},\,Pd/PbC{O_3}}}$ CH3-CH=CH2(g)
Hãy tính biến thiên enthalpy của phản ứng tạo thành propene trên biết rằng năng lượng liên kết đo ở điều kiện chuẩn của một số liên kết như sau:
| Liên kết | H – H | C – H | C – C | C = C | C ≡ C |
| Eb (kJ/mol) | 432 | 413 | 347 | 614 | 839 |
Câu 6. Khi đốt cháy 1 mol propane toả ra lượng nhiệt là 2 220 kJ. Để đun nóng 1 gam nước tăng thêm 1 °C cần cung cấp nhiệt lượng là 4,2 J. Tính khối lượng propane cần dùng để đun 1L nước từ 25 °C lên 100 °C. Cho biết 75% nhiệt lượng toả ra khi đốt cháy propane dùng để nâng nhiệt độ của nước. Khối lượng riêng của nước là 1 g/mL. (Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN
PHẦN I (4,5 đ). Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ Câu 1 đến câu 18. Mỗi Câu hỏi thí sinh chỉ chọn một phương án. Mỗi Câu trả lời đúng thí sinh được 0,25 đ
| 1 | 2 | 3 | 4 | 5 | 6 |
| B | D | A | A | C | C |
| 7 | 8 | 9 | 10 | 11 | 12 |
| D | C | B | A | D | B |
| 13 | 14 | 15 | 16 | 17 | 18 |
| B | B | A | C | B | D |
PHẦN II (4 đ). Câu trắc nghiệm đúng sai. Thí sinh trả lời từ Câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi Câu, thí sinh chọn đúng hoặc sai.
-Điểm tối đa của 01 Câu hỏi là 1 điểm
-Thí sinh lựa chọn chính xác 01 ý trong 1 Câu hỏi được 0,1 điểm
-Thí sinh lựa chọn chính xác 02 ý trong 1 Câu hỏi được 0,25 điểm
-Thí sinh lựa chọn chính xác 03 ý trong 1 Câu hỏi được 0,5 điểm
-Thí sinh lựa chọn chính xác 04 ý trong 1 Câu hỏi được 1 điểm
| Câu | Lệnh hỏi | Đáp án (Đ/S) |
Câu | Lệnh hỏi | Đáp án (Đ/S) |
| 1 | a | Đ | 3 | a | Đ |
| b | S | b | Đ | ||
| c | Đ | c | Đ | ||
| d | Đ | d | S | ||
| 2 | a | Đ | 4 | a | S |
| b | Đ | b | Đ | ||
| c | Đ | c | Đ | ||
| d | S | d | S |
PHẦN III (1,5 đ): Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ Câu 1 đến câu 6.
Mỗi Câu đúng 1,5 điểm
Mỗi Câu trả lời đúng thí sinh được 0,25 điểm
| Câu | 1 | 2 | 3 | 4 | 5 | 6 |
| ĐA | 92,9 | 26 | 25,6 | 2,8 | -169 | 8,3 |
HƯỚNG DẪN GIẢI
PHẦN III: Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ Câu 1 đến Câu 6.
Câu 1. Tính chỉ số octane của xăng E5, biết xăng E5 chứa 5% ethanol và 95% xăng RON 92 (theo thể tích). (Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN 92,9
Trong 100 L xăng E5 có 95 L xăng RON 92 và 5 L ethanol.
Chỉ số octane của xăng E5 là $\frac{{95.92 + 5.109}}{{100}} = 92,85$.
Câu 2. Phân tích thành phần nguyên tố của hợp chất hữu cơ X thu được kết quả %C và %H (theo khối lượng) lần lượt là 84,21% và 15,79%. Phân tử khối của hợp chất X này được xác định thông qua kết quả phổ khối lượng như hình bên dưới với peak ion phân tử có giá trị m/z lớn nhất.
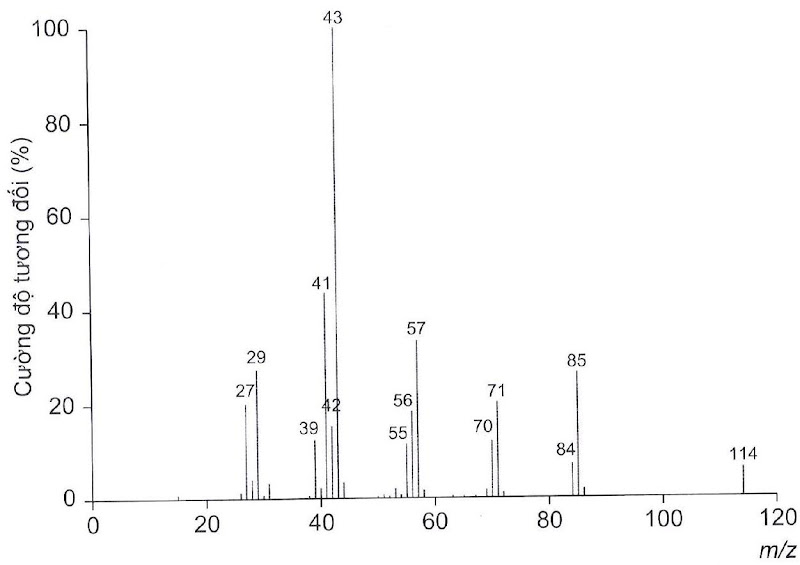
Tổng số nguyên tử trong phân tử của X là bao nhiêu?
ĐÁP ÁN 26
Vì %mC + %mH = 100% nên phân tử X chỉ chứa các nguyên tố hydrogen và carbon.
Đặt công thức phân tử của X là CxHy , ta có: $x:y = \frac{{\% C}}{{12}}:\frac{{\% H}}{1} = \frac{{84,21}}{{12}}:\frac{{15,79}}{1} = 7,0175:15,79 = 4:9$
Vậy công thức phân tử của X có dạng (C4H9)n .
Phổ khối lượng của X cho thấy X có phân tử khối là 114.
${M_{(X)}} = 114 \Leftrightarrow 57n = 114 \Rightarrow n = 2$.
Do đó công thức phân tử của X là C8H18.
Câu 3: Đun sôi 15,7 gam C3H7Cl với hỗn hợp KOH/C2H5OH dư, sau khi loại tạp chất và dẫn khí sinh ra qua dung dịch bromine dư thấy có x gam Br2 tham gia phản ứng. Tính x nếu hiệu suất phản ứng ban đầu là 80%. (Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN 25,6
Phương trình phản ứng :
C3H7Cl$\xrightarrow{{KOH/{C_2}{H_5}OH,\,{t^0}}}$ C3H6 + HCl (1)
mol: 0,2.80% → 0,16
C3H6 + Br2 → C3H6Br2 (2)
mol: 0,16 → 0,16
Theo các phản ứng và giả thiết ta có : x = 0,16.160 = 25,6 gam.
Câu 4: Hiện nay PVC được điều chế theo sơ đồ sau:
C2H4 → CH2Cl–CH2Cl → C2H3Cl → PVC.
Nếu hiệu suất toàn bộ quá trình đạt 80% thì lượng C2H4 cần dùng là bao nhiêu tấn để sản xuất 5 tấn PVC? (Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN 2,8
Hướng dẫn giải
Khối lượng C2H4 cần dùng = $\frac{5}{{62,5n}} \cdot 28n \cdot \frac{{100}}{{80}} = 2,8$ (tấn)
Câu 5. Propene là nguyên liệu cho sản xuất nhựa polypropylene (PP). PP được sử dụng để sản xuất các sản phẩm ống, màng, dây cách điện, kéo sợi, đồ gia dụng và các sản phẩm tạo hình khác.
Phản ứng tạo thành propene từ propyne:
CH3-C≡CH(g) + H2(g) $\xrightarrow{{{t^0},\,Pd/PbC{O_3}}}$ CH3-CH=CH2(g)
Hãy tính biến thiên enthalpy của phản ứng tạo thành propene trên biết rằng năng lượng liên kết đo ở điều kiện chuẩn của một số liên kết như sau:
| Liên kết | H – H | C – H | C – C | C = C | C ≡ C |
| Eb (kJ/mol) | 432 | 413 | 347 | 614 | 839 |
ĐÁP ÁN -169
Hướng dẫn giải
(b) Biến thiên enthalpy của phản ứng: CH3-C≡CH(g) + H2(g) $\xrightarrow[{Pd/PbC{O_3}}]{{{t^0}}}$CH3-CH=CH2(g)
${\Delta _f}H_{298}^0$= Eb(C≡C) + Eb(C-C) + 4xEb(C-H) + Eb(H-H) – Eb(C=C) – Eb(C-C) – 6xEb(C-H)
= 839 + 347+ 4×413 + 432-614-347-6×413 = -169 kJ
Câu 6. Khi đốt cháy 1 mol propane toả ra lượng nhiệt là 2 220 kJ. Để đun nóng 1 gam nước tăng thêm 1 °C cần cung cấp nhiệt lượng là 4,2 J. Tính khối lượng propane cần dùng để đun 1L nước từ 25 °C lên 100 °C. Cho biết 75% nhiệt lượng toả ra khi đốt cháy propane dùng để nâng nhiệt độ của nước. Khối lượng riêng của nước là 1 g/mL. (Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN 8,3
Hướng dẫn giải
Nhiệt lượng cần cung cấp trên lí thuyết để đun nóng 1 L nước hay 1 000 gam nước từ 25 °C lên 100 °C là:
Q = m.C.∆T= 1 000 (g) x (100 – 25) (oC) x 4,2 (J/oC.g) = 315 000 (J) = 315 (kJ).
Khối lượng propane thực tế cần lấy: $ = \frac{{44 \times 315}}{{2220}} \cdot \frac{{100}}{{75}} \approx 8,3(\;g)$