Đề ôn thi HK2 Hóa 11 Chân trời sáng tạo giải chi tiết-Đề 2 được soạn dưới dạng file word và PDF gồm 4 trang. Các bạn xem và tải về ở dưới.
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Alkane là những hydrocarbon no, mạch hở, có công thức chung là
A. CnH2n+2 (n ≥1). B. CnH2n (n ≥2). C. CnH2n-2 (n ≥2). D. CnH2n-6 (n ≥6).
Câu 2. Acetylene (ethyne) có công thức phân tử là
A. CH4. B. C2H4. C. C2H2. D. C3H6.
Câu 3. Alkene Y có tổng số liên kết σ trong phân tử là 11. Số đồng phân cấu tạo của X là
A. 1. B. 2. C. 3. D. 4.
Câu 4. Ở điều kiện thích hợp, alkene tác dụng với chất nào sau đây tạo thành alcohol?
A. H2. B. HCl. C. H2O. D. Br2.
Câu 5. Chất nào là dẫn xuất halogen của hydrocarbon?
A. Cl – CH2 – COOH. B. C6H5 – CH2 – Cl. C. CH2OH – CH2 – Br. D. CH3 – CO – Cl.
Câu 6. Cho các dẫn xuất halogen sau: (1) C2H5F; (2) C2H5Cl; C2H5Br (3) ; C2H5I (4) . Thứ tự giảm dần nhiệt độ sôi là
A. (1) > (2) > (3) > (4). B. (1) > (4) > (2) >(3)
C. (4) > (3) > (2) > (1). D. (4) > (2) > (1) > (3).
Câu 7. Cồn 700 được sử dụng phổ biến trong y tế, dùng để sát trùng, diệt khuẩn,. Cách pha chế cồn 700 là
A. pha 70 ml nước với 30 ml ethanol.
B. pha 70 ml ethanol với 30 ml nước.
C. lấy 70 ml rồi thêm 100 ml nước.
D. lấy 70 ml ethanol rồi thêm nước để thu được 100 ml cồn.
Câu 8. Công thức phân tử của ethyl alcohol là
A. C3H8O3. B. CH4O. C. C2H6O. D. C2H4O2.
Câu 9. Methyl alcohol, ethyl alcohol tan vô hạn trong nước là do
A. khối lượng phân tử của các alcohol nhỏ.
B. hình thành tương tác van der Waals với nước.
C. hình thành liên kết hydrogen với nước.
D. hình thành liên kết cộng hoá trị với nước.
Câu 10. Sản phẩm chính thu được khi tách nước từ 3-methylbutan-2-ol là
A. 3-metylbut-1-ene. B. 2-methylbut-2-ene.
C. 3-methylbut-2-ene. D. 2-methylbut-3-ene.
Câu 11. Đun nóng methanol với H2SO4 đặc ở 140 oC thu được sản phẩm chính là
A. C2H5OSO3H. B. C2H4. C. C2H5OC2H5. D. CH3OCH3.
Câu 12. Trong đặc điểm cấu tạo của phenol, cặp electron trên nguyên tử oxygen bị hút một phần vào hệ thống vòng benzene, làm giàu mật độ electron ở các vị trí
A. ortho, meta. B. meta, para.
C. ortho, meta, para. D. ortho, para.
Câu 13. Phản ứng với chất/dung dịch nào sau đây của phenol chứng minh phenol có tính acid?
A. Na. B. Dung dịch NaOH.
C. Dung dịch bromine. D. HNO3 đặc/ H2SO4 đặc.
Câu 14. Tính chất vật lý nào đặc trưng cho formic aldehyde
A. Là chất lỏng không màu, có mùi thơm, tan tốt trong nước.
B. Là chất khí, không màu, có mùi xốc, tan tốt trong nước.
C. Là chất lỏng không màu, có mùi xốc, tan ít trong nước.
D. Là chất khí không màu, có mùi xốc, tan ít trong nước.
Câu 15. Khử hợp chất hữu cơ X bằng LiAlH4, thu được (CH3)2CH-CH2-CH2OH.
Chất X có tên là
A. 3-methylbutanal. B. 2-methylbutan-3-al.
C. 2-methylbutanal. D. 3-methylbutan-3-al.
Câu 16. Không thể phân biệt aldehyde fomic và acetone bằng phản ứng với
A. dung dịch brom. B. dung dịch KMnO4.
C. thuốc thử Tollens. D. H2 (xúc tác: Ni, t0).
Câu 17. Hợp chất X có công thức cấu tạo: (CH3)2CHCH2COOH. Tên của X là
A. 2 – methylpropanoic acid. B. 2 – methylbutanoic acid.
C. 3 – methylbutanoic acid. D. 3 – methylbutan – 1 – oic acid.
Câu 18. Vị chua của giấm là do chứa
A. acetic acid. B. salicylic acid. C. oxalic acid. D. citric acid.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.

Câu 1. Dẫn xuất halogen có nhiều ứng dụng trong các ngành công nghiệp như: làm dung môi, là chất trung gian để tổng hợp chất hữu cơ như: alcohol, phenol,… ; là chất đầu để tổng hợp polymer CH2 =CHCl tổng hợp poly(vinyl chloride) – PVC;…
a. Ở điều kiện thường, các chất CH3F, CH3Cl và CH3Br ở thể khí.
b. Phần lớn dẫn xuất halogen nhẹ hơn nước và hầu như không tan trong nước và tan tốt các dung môi hữu cơ.
c. Một số dẫn xuất halogen có hoạt tính sinh học cao như: chloroform, ethyl chloride, ethyl bromide,…
d. Các hợp chất chỉ chứa chlorine, fluorine và carbon trong phân tử được gọi chung là các hợp chất CFC.
Câu 2. Alcohol là những hợp chất hữu cơ trong phân tử có nhóm hydroxy (-OH) liên kết trực tiếp với nguyên tử carbon no.
a. Alcohol no, đơn chức, mạch hở có công thức chung là CnH2n+1OH (n≥1).
b. Glycerol hòa tan được copper (II) hydroxide tạo thành phức chất màu tím .
c. Benzyl alcohol thuộc loại alcohol đa chức.
d. Nhiều vụ ngộ độc rượu do sử dụng rượu được pha chế từ cồn công nghiệp có lẫn methanol.
Câu 3. Methacrylic acid được dùng trong tổng hợp thủy tinh hữu cơ.
a. Methacrylic acid thuộc dãy đồng đẳng của acetic acid.
b. Methacrylic acid làm mất màu nước bromine.
c. Phân tử khối của methacrylic acid là 88.
d. Dung dịch methacrylic acid làm quỳ tím hóa đỏ.
Câu 4. Aldehyde và ketone thuộc loại hợp chất carbonyl chứa liên kết đôi C=O trong phân tử.
a. Aldehyde phản ứng được với nước bromine.
b. Ketone phản ứng được với Cu(OH)2/OH–.
c. Aldehyde tác dụng với dung dịch AgNO3/NH3 tạo ra bạc.
d. Trong các hợp chất carbonyl, chỉ aldehyde bị khử bởi NaBH4.
PHẦN III: Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Số đồng phân carboxylic acid có công thức phân tử C4H8O2 là bao nhiêu?
Câu 2. Cho các thí nghiệm:
(a) Đun nóng C6H5CH2Cl trong dung dịch NaOH.
(b) Đung nóng hỗn hợp CH3CH2CH2Cl, KOH và C2H5OH.
(c) Đun nóng CH3CH2CH2Cl trong dung dịch NaOH.
(d) Đun nóng hỗn hợp CH3CHClCH=CH2, KOH và C2H5OH.
Có bao nhiêu thí nghiệm tạo sản phẩm chính là alcohol?
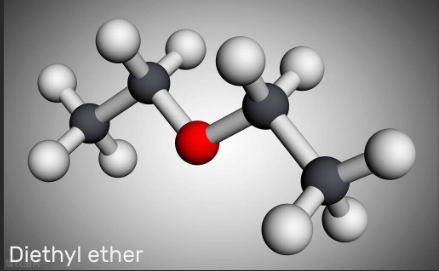
Câu 3. Diethyl ether là hợp chất hữu cơ có công thức C2H5OC2H5 (viết tắt là Et2O) thường được sử dụng làm dung môi không proton phổ biến trong phòng thí nghiệm, dung môi đặc biệt quan trọng trong sản xuất nhựa cellulose như cellulose acetate. Et2O được sản xuất bằng phương pháp loại nước ở thể hơi ethyl alcohol với xúc tác alumina (Al2O3), hiệu suất lên đến 95%
Theo tính toán lí thuyết, để sản xuất 74 kg diethyl ether, cần khối lượng ethyl alcohol tối thiểu là bao nhiêu kg? (Cho NTK: H=1, C=12, O=16).
(Làm tròn kết quả đến hàng phần mười)
Câu 4. Một đơn vị cồn tương đương 10 g cồn (ethalnol) nguyên chất. Theo khuyến cáo của ngành y tế, để đảm bảo sức khỏe mỗi người trưởng thành không nên uống quá 2 đơn vị cồn mỗi ngày. Vậy mỗi người trưởng thành không nên uống quá bao nhiêu mL rượu 400 một ngày?

Biết ${D_{{C_2}{H_5}OH}} = 0,8\;g/mL$. (Cho NTK: H=1, C=12, O=16).
(Làm tròn kết quả đến hàng phần mười).
Vậy mỗi người trưởng thành không nên uống quá 62,5 mL rượu 400 một ngày
Câu 5. Cho 20 gam dung dịch acetaldehyde tác dụng với lượng dư dung dịch AgNO3 trong NH3, thu được 21,6 gam Ag. Tính nồng độ phần trăm của acetaldehyde trong dung dịch đã sử dụng. (Cho NTK: H=1, C=12, O=16, N=14, Ag=108). (Làm tròn kết quả đến hàng phần mười).
Câu 6. Cho 12 g acetic acid phản ứng với 12 g ethanol (có H2SO4 đặc làm xúc tác) thu được 8,8 g ester. Tính hiệu suất phản ứng ester hoá. (Cho NTK: H=1, C=12, O=16).
(Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN VÀ LỜI GIẢI
PHẦN I (4,5 đ). Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Mỗi câu trả lời đúng thí sinh được 0,25 đ
| 1 | 2 | 3 | 4 | 5 | 6 |
| A | C | C | C | B | C |
| 7 | 8 | 9 | 10 | 11 | 12 |
| D | C | C | B | D | D |
| 13 | 14 | 15 | 16 | 17 | 18 |
| B | B | A | D | C | A |
PHẦN II (4 đ). Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
| Câu | Lệnh hỏi | Đáp án (Đ/S) |
Câu | Lệnh hỏi | Đáp án (Đ/S) |
| 1 | a | Đ | 3 | a | S |
| b | S | b | Đ | ||
| c | Đ | c | S | ||
| d | Đ | d | Đ | ||
| 2 | a | Đ | 4 | a | Đ |
| b | S | b | S | ||
| c | S | c | Đ | ||
| d | Đ | d | S |
PHẦN III (1,5 đ): Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
| Câu | 1 | 2 | 3 | 4 | 5 | 6 |
| ĐA | 2 | 2 | 48,4 | 62,5 | 22 | 50 |
HƯỚNG DẪN GIẢI
PHẦN III: Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Số đồng phân carboxylic acid có công thức phân tử C4H8O2 là bao nhiêu?
ĐÁP ÁN: 2
Câu 2. Cho các thí nghiệm:
(a) Đun nóng C6H5CH2Cl trong dung dịch NaOH.
(b) Đung nóng hỗn hợp CH3CH2CH2Cl, KOH và C2H5OH.
(c) Đun nóng CH3CH2CH2Cl trong dung dịch NaOH.
(d) Đun nóng hỗn hợp CH3CHClCH=CH2, KOH và C2H5OH.
Có bao nhiêu thí nghiệm tạo sản phẩm chính là alcohol?
ĐÁP ÁN: 2
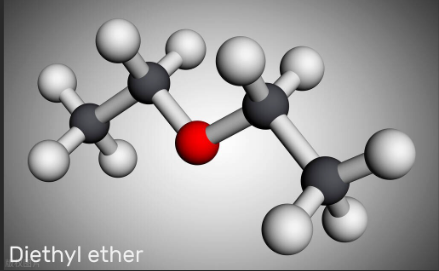
Câu 3. Diethyl ether là hợp chất hữu cơ có công thức C2H5OC2H5 (viết tắt là Et2O) thường được sử dụng làm dung môi không proton phổ biến trong phòng thí nghiệm, dung môi đặc biệt quan trọng trong sản xuất nhựa cellulose như cellulose acetate. Et2O được sản xuất bằng phương pháp loại nước ở thể hơi ethyl alcohol với xúc tác alumina (Al2O3), hiệu suất lên đến 95%
Theo tính toán lí thuyết, để sản xuất 74 kg diethyl ether, cần khối lượng ethyl alcohol tối thiểu là bao nhiêu kg? (Cho NTK: H=1, C=12, O=16).
(Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN: 48,4
Hướng dẫn giải
Phương trình hoá học của phản ứng:
$2{C_2}{H_5}OH\xrightarrow{{A{l_2}{O_3}}}{C_2}{H_5}O{C_2}{H_5} + {H_2}O$
${n_{{C_2}{H_5}O{C_2}{H_5}}} = {10^3}\;mol$
${m_{{C_2}{H_5}OH}} = {10^3}\frac{{100}}{{95}} \cdot 46 = gam$= 48421,05 gam ≈ 48,4 kg
Câu 4. Một đơn vị cồn tương đương 10 g cồn (ethalnol) nguyên chất. Theo khuyến cáo của ngành y tế, để đảm bảo sức khỏe mỗi người trưởng thành không nên uống quá 2 đơn vị cồn mỗi ngày. Vậy mỗi người trưởng thành không nên uống quá bao nhiêu mL rượu 400 một ngày? Biết ${D_{{C_2}{H_5}OH}} = 0,8\;g/mL$. (Cho NTK: H=1, C=12, O=16).
(Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN: 62,5
Hướng dẫn giải
methanol tối đa 1 ngày = 10.2 = 20 gam $ \Rightarrow $Vethanol 20 : 0,8 = 25 mL $ \Rightarrow {V_{ruou{{40}^0}}} = \frac{{25.100}}{{40}} = 62,5(\;mL)$
Vậy mỗi người trưởng thành không nên uống quá 62,5 mL rượu 400 một ngày
Câu 5. Cho 20 gam dung dịch acetaldehyde tác dụng với lượng dư dung dịch AgNO3 trong NH3, thu được 21,6 gam Ag. Tính nồng độ phần trăm của acetaldehyde trong dung dịch đã sử dụng. (Cho NTK: H=1, C=12, O=16, N=14, Ag=108). (Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN: 22
Hướng dẫn giải
PTHH:
![]()
${n_{Ag}} = 21,8:108 = 0,2\;mol \Rightarrow {n_{C{H_3}CHO}} = 0,1\;mol$
$ \Rightarrow {C_{\left( {C{H_3}CHO} \right)}} = \frac{{0,1 \cdot 44}}{{20}} \cdot 100\% = 22\% $
Câu 6. Cho 12 g acetic acid phản ứng với 12 g ethanol (có H2SO4 đặc làm xúc tác) thu được 8,8 g ester. Tính hiệu suất phản ứng ester hoá.
ĐÁP ÁN: 50
Hướng dẫn giải
${n_{C{H_3}OOH}} = \frac{{12}}{{60}} = 0,2\;mol$ ; ${n_{{C_2}{H_5}OH}} = \frac{{12}}{{46}}$ ; ${n_{C{H_3}OO{C_2}{H_5}}} = \frac{{8,8}}{{88}} = 0,1\;mol$
PTHH:CH3COOH+C2H5OH⇌CH3COOC2H5+H2O
So sánh tỉ lệ thì số mol C2H5OH dư, hiệu suất tính theo CH3COOH
$H\% = \frac{{0,1}}{{0,2}} \cdot 100 = 50\% $