Đề thi giữa học kỳ 2 Hóa 11 CTST cấu trúc mới giải chi tiết-Đề 3 được soạn dưới dạng file word và PDF gồm 4 trang. Các bạn xem và tải về ở dưới.
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Dãy nào sau đây chỉ gồm các alkane?
A. C2H2, C3H4, C4H6, C5H8. B. CH4, C2H2, C3H4, C4H10.
C. CH4, C2H6, C4H10, C5H12. D. C2H6, C3H8, C5H10, C6H12.
Câu 2. Cho dãy các alkane: butane, isobutane, isopentane, neopentane. Alkane nào trong dãy có chứa nguyên tử carbon bậc IV?
A. Isobutane. B. Butane. C. Neopentane. D. Isopentane.
Câu 3. Nhiệt độ sôi của ba alkane là đồng phân cấu tạo của nhau, có cùng công thức phân tử C5H12 là 36 oC, 28 oC và 9,4 oC. Các alkane ứng với thứ tự nhiệt độ sôi ở trên lần lượt là
A. neopentane, isopentane, pentane.
B. pentane, neopentane, isopentane.
C. pentane, isopentane, neopentane.
D. isopentane, neopentane, pentane.
Câu 4. Sự tách hydrogen halogenua của dẫn xuất halogen X có công thức phân tử C4H9Cl cho một alkene không phân nhánh duy nhất, X là chất nào trong những chất sau đây ?
A. 1-chlorobutane. B. 1-chloro-2-methylpropane.
C. 2-chloro-2-methylpropane. D. 2-chlorobutane.
Câu 5. Điều kiện để alkene có đồng phân hình học?
A. Mỗi nguyên tử carbon ở liên kết đôi liên kết với hai nguyên tử hoặc nhóm nguyên tử bất kì.
B. Mỗi nguyên tử carbon ở liên kết đôi liên kết với hai nguyên tử hoặc nhóm nguyên tử khác nhau.
C. Mỗi nguyên tử carbon ở liên kết đôi liên kết với hai nguyên tử hoặc nhóm nguyên tử giống nhau.
D. 4 nguyên tử hoặc nhóm nguyên tử ở hai nguyên tử carbon mang nối đôi phải khác nhau.
Câu 6. Tên thay thế alkyne có công thức HC ≡ C – CH2 – CH3 là
A. But-1-ene B. But-2-ene C. But-1-yne D. But-2-yne
Câu 7. Trong phân tử acetylene liên kết ba C ≡ C giữa 2 carbon gồm
A. 1 liên kết pi (π) và 2 liên kết xích ma (σ). B. 2 liên kết pi (π) và 1 liên kết xích ma (σ).
C. 2 liên kết pi (π) và 2 liên kết xích ma (σ). D. 3 liên kết pi (π) và 2 liên kết xích ma (σ).
Câu 8. Các alkene không có các tính chất vật lí đặc trưng nào sau đây?
A. Tan tốt trong nước và các dung môi hữu cơ.
B. Có khối lượng riêng nhỏ hơn khối lượng riêng của nước.
C. Có nhiệt độ sôi thấp hơn alkane phân tử có cùng số nguyên tử carbon.
D. Không dẫn điện.
Câu 9. Phản ứng đặc trưng của alkene là
A. phản ứng cộng B. phản ứng tách C. phản ứng thế D. phản ứng oxi hóa
Câu 10. Alkene + H2 dư $\xrightarrow{{Ni,\,{t^0}}}$ X
Chất X là
A. alkane B. alkene C. alkyne D. alk-1yne
Câu 11. Chất nào sau đây làm mất màu dung dịch bromine?
A. Butane. B. But-1-ene. C. Carbon dioxide D. Methylpropane.
Câu 12. Cho các chất sau: (X) o-bromotoluene; (Y) m-bromotoluene; (Z) p-bromotoluene. Sản phẩm chính của phản ứng giữa toluene với bromine ở nhiệt độ cao có mặt iron(III) bromide là
A. (X) và (Y). B. (Y) và (Z). C. (X) và (Z). D. (Y).
Câu 13. Sản phẩm tạo thành khi cho benzene tác dụng với HNO3 đặc có H2SO4 đ; t0 ( tỉ lệ mol 1:1), là:
A. nitrobenzene B. o-dinitrobenzene C. m-dinitrobenzene D. p-dinitrobenzene
Câu 14. Chlorine phản ứng với toluene sôi dưới ánh sáng UV (không có xúc tác) phản ứng thường nhận được hỗn hợp các sản phẩm dù bất kì ở tỉ lệ nào của toluene với chlorine. Trong số các sản phẩm thu được có sản phẩm là
A. p-chlorotoluene. B. benzyl chloride.
C. m-chlorotoluene. D.2,4-dichlorotoluene.
Câu 15. Chất nào sau đây thuộc loại dẫn xuất halogen của hydrocarbon?
A.C2H5OH. B. CH3CHO. C. CH3Cl. D. C2H7N.
Câu 16. Dẫn xuất halogen không có đồng phân cis-trans là
A. CHCl=CHCl. B. CH2=CH-CH2F.
C. CH3CH=CBrCH3. D.CH3CH2CH=CHCHClCH3.
Câu 17. Sản phẩm chính của phản ứng giữa propene và dung dịch nước chlorine (Cl2 + H2O) là
A. CH3-CHCl-CH3. B. CH3-CH(OH)-CH3.
C. CH3-CHCl-CH2OH. D. CH3-CH(OH)-CH2Cl
Câu 18. Nhỏ dung dịch AgNO3 vào ống nghiệm chứa một ít dẫn xuất halogen CH2=CHCH2Cl, lắc nhẹ. Hiện tượng xảy ra là
A. Thoát ra khí màu vàng lục. B. xuất hiện kết tủa trắng.
C. không có hiện tượng. D. xuất hiện kết tủa vàng.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1. Alkane là những hydrocarbon mạch hở, phân tử chỉ chứa liên kết đơn.
a. Tất cả các alkane đều có công thức chung là CnH2n+2 (n ≥ 1).
b. Ở nhiệt độ thường, các alkane khá hoạt động hóa học.
c. Các alkane đều nặng hơn nước.
d. Tất cả các chất chỉ chứa liên kết đơn trong phân tử đều là alkane.
Câu 2. Alkane có nhiều ứng dụng trong đời sống và trong công nghiệp.
a. Propane C3H8 và butane C4H10 được sử dụng làm khí đốt.
b. Các alkane C6, C7, C8 là nguyên liệu để sản xuất một số hydrocarbon thơm.
b. Các alkane lỏng được sử dụng làm nhiên liệu như xăng hay dầu diesel.
d. Các alkane từ C11 đến C20 được dùng làm nến và sáp.
Câu 3. Nhu cầu sử dụng PVC trên toàn thế giới liên tục tăng trong các năm qua, người ta tổng hợp PVC từ vinyl chloride.
a. PVC là từ viết tắt của poly(vinyl chloride).
b. PVC được dùng làm ống nước, vỏ bọc dây điện, vải giả da,…
c. Để thu được PVC người ta tiến hành cho vinyl chloride tác dụng với dung dịch NaOH đun nóng.
d. Có thể điều chế vinyl chloride từ acetylene hoặc ethylene.
Câu 4. Tiến hành thí nghiệm phản ứng của hexane với bromine như sau:
Bước 1: Cho vào ống nghiệm khô khoảng 1 ml hexane và nhỏ tiếp vào ống nghiệm khoảng 1 ml nước bromine.
Bước 2: Nút ống nghiệm bằng bông tẩm dung dịch NaOH.
Bước 3: Lắc nhẹ hỗn hợp phản ứng rồi nhúng vào cốc nước nóng 50oC.
a. Sau bước 1, chất lỏng trong ống nghiệm đồng nhất.
b. Sau bước 3, màu nước bromine nhạt dần và có thể mất mất màu hoàn toàn.
c. Sau bước 3, chất lỏng trong ống nghiệm tách thành 2 lớp, lớp trên là nước.
d. Có thể thay việc ngâm trong nước nóng 50oC bằng cách để ra ngoài ánh sáng mặt trời.
PHẦN III: Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Hợp chất X có công thức cấu tạo thu gọn được biểu diễn ở hình bên.
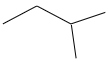
Tổng số nguyên tử C và H trong phân tử X là bao nhiêu?
Câu 2. Các alkene và alkyne từ mấy C trở lên có đồng phân vị trí liên kết bội?
Câu 3. Ứng với các công thức C8H10 có bao nhiêu đồng phân hydrocarbon thơm?
Câu 4. Hydrocarbon Y có công thức cấu tạo như sau: (CH3)2CHCH2CH3. Khi cho Y phản ứng với bromine có thể thu được bao nhiêu dẫn xuất monobromo là đồng phân cấu tạo của nhau?
Câu 5. Hấp thụ hoàn toàn 0,05 mol hỗn hợp X (gồm 2 alkyne là đồng đẳng kế tiếp) vào bình đựng dung dịch Br2 dư. Kết thúc thí nghiệm, khối lượng bình Br2 tăng thêm 1,79 gam. Xác định công thức phân tử của hai alkyne. Phân trăm theo số mol của alkyne có phân tử khối nhỏ hơn là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
Câu 6. Đun nóng 27,40 gam CH3CHBrCH2CH3 với NaOH dư trong C2H5OH, sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp khí X gồm hai alkene trong đó sản phẩm chính chiếm 80%, sản phẩm phụ chiếm 20%. Đốt cháy hoàn toàn X thu được bao nhiêu lít CO2 (đkc) ? Biết các phản ứng xảy ra với hiệu suất phản ứng là 100%. (Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN
PHẦN I (4,5 đ). Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Mỗi câu trả lời đúng thí sinh được 0,25 đ
| 1 | 2 | 3 | 4 | 5 | 6 |
| C | C | C | A | B | C |
| 7 | 8 | 9 | 10 | 11 | 12 |
| B | A | A | A | B | C |
| 13 | 14 | 15 | 16 | 17 | 18 |
| A | B | C | B | D | C |
PHẦN II (4 đ). Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
-Điểm tối đa của 01 câu hỏi là 1 điểm
-Thí sinh lựa chọn chính xác 01 ý trong 1 câu hỏi được 0,1 điểm
-Thí sinh lựa chọn chính xác 02 ý trong 1 câu hỏi được 0,25 điểm
-Thí sinh lựa chọn chính xác 03 ý trong 1 câu hỏi được 0,5 điểm
-Thí sinh lựa chọn chính xác 04 ý trong 1 câu hỏi được 1 điểm
| Câu | Lệnh hỏi | Đáp án (Đ/S) |
Câu | Lệnh hỏi | Đáp án (Đ/S) |
| 1 | a | Đ | 3 | a | Đ |
| b | S | b | Đ | ||
| c | S | c | S | ||
| d | S | d | Đ | ||
| 2 | a | Đ | 4 | a | S |
| b | Đ | b | Đ | ||
| c | Đ | c | S | ||
| d | S | d | Đ |
PHẦN III (1,5 đ): Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6. Mỗi câu đúng 1,5 điểm
Mỗi câu trả lời đúng thí sinh được 0,25 điểm
| Câu | 1 | 2 | 3 | 4 | 5 | 6 |
| ĐA | 17 | 4 | 4 | 4 | 30 | 19,8 |
HƯỚNG DẪN GIẢI
PHẦN III: Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Hợp chất X có công thức cấu tạo thu gọn được biểu diễn ở hình bên.
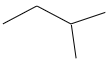
Tổng số nguyên tử C và H trong phân tử X là bao nhiêu?
ĐÁP ÁN LÀ 17
Câu 2. Các alkene và alkyne từ mấy C trở lên có đồng phân vị trí liên kết bội?
ĐÁP ÁN LÀ 4
Câu 3. Ứng với các công thức C8H10 có bao nhiêu đồng phân hydrocarbon thơm?
ĐÁP ÁN LÀ 4
Câu 4. Hydrocarbon Y có công thức cấu tạo như sau: (CH3)2CHCH2CH3. Khi cho Y phản ứng với bromine có thể thu được bao nhiêu dẫn xuất monobromo là đồng phân cấu tạo của nhau?
ĐÁP ÁN LÀ 4
Câu 5. Hấp thụ hoàn toàn 0,05 mol hỗn hợp X (gồm 2 alkyne là đồng đẳng kế tiếp) vào bình đựng dung dịch Br2 dư. Kết thúc thí nghiệm, khối lượng bình Br2 tăng thêm 1,79 gam. Xác định công thức phân tử của hai alkyne. Phân trăm theo số mol của alkyne có phân tử khối nhỏ hơn là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN LÀ 30
Hướng dẫn giải
Gọi CTPT của alkane là CnH2n-2 (n ≥ 2)
Khối lượng bình Br2 tăng thêm=khối lượng alkyne tham gia phản ứng=1,79 gam.
${M_{{C_{\overline n }}{H_{2\overline n }}}} = \frac{{1,79}}{{0,05}} = 35,8$
$ \Rightarrow 12\overline n + 2\overline n – 2 = 35,8 \Rightarrow \overline n = 2,7$
Vậy CTPT của 2 alkyne cần tìm là C2H2 và C3H4.
Chọn số mol hỗn hợp = 1 mol
Đặt n C2H2 = a mol và n =C3H4 = b mol
a +b =1
2a + 3b =2,7
a=0,3 và b=0,7 → %n C2H2 = 30%
Câu 6: Đun nóng 27,40 gam CH3CHBrCH2CH3 với NaOH dư trong C2H5OH, sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp khí X gồm hai alkene trong đó sản phẩm chính chiếm 80%, sản phẩm phụ chiếm 20%. Đốt cháy hoàn toàn X thu được bao nhiêu lít CO2 (đkc) ? Biết các phản ứng xảy ra với hiệu suất phản ứng là 100%. (Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN LÀ 19,8
Hướng dẫn giải
Khi đun nóng CH3CHBrCH2CH3 với KOH dư trong C2H5OH thì thu được hai sản phẩm hữu cơ là but-1-en và but-2-en.
Phương trình phản ứng :
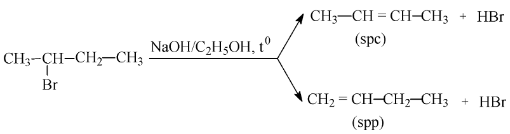
C4H8 + 6O2 $\xrightarrow{{{t^0}}}$4CO2 + 4H2O
Theo các phương trình phản ứng và giả thiết ta thấy :
${n_{C{O_2}}} = 4 \cdot {n_{{C_4}{H_8}}} = 4 \cdot {n_{C{H_3}CHBrC{H_2}C{H_3}}} = 4 \cdot \frac{{27,4}}{{137}} = 4 \cdot 0,2 = 0,8\;mol$.
Vậy ${V_{C{O_2}}}$= 0,8.24,79 = 19,832 lít.