Đề cương ôn giữa học kỳ 2 Hóa 11 Chân trời sáng tạo có đáp án được soạn dưới dạng file word và PDF gồm 4 trang. Các bạn xem và tải về ở dưới.
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ Câu 1 đến Câu 18. Mỗi Câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Bậc của nguyên tử carbon đánh dấu (*) trong hợp chất sau là
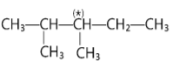
A. bậc I. B. bậc II. C. bậc III. D. bậc IV.
Câu 2. Cracking hoàn toàn butane với xúc tác thích hợp, nếu thu được methane và một alkene X thì công thức cấu tạo thu gọn của X là
A. CH3-CH2-CH=CH2. B. CH3−CH=CH2.
C. CH2=CH2. D. CH3−CH=CH−CH3.
Câu 3. Phát biểu nào sau đây không đúng?
A. Alkane không tan trong dung dịch NaOH hoặc H2SO4.
B. Alkane tan tốt trong nước.
C. Các alkane từ C1 đến C4 là chất khí.
D. Các alkane nhẹ như methane, ethane, propane là những khí không màu.
Câu 4. Alkene sau có tên là gì
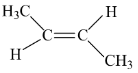
A. but-2-ene B. cis-but-2-ene C. trans-but-2-ene D. but-1-ene
Câu 5. Cho các chất sau: chloromethane, dichloromethane, trichloromethane và tetrachloromethane. Số chất là sản phẩm của phản ứng xảy ra khi trộn methane với chlorine và chiếu ánh sáng từ ngoại là
A. 1. B. 2. C. 3. D. 4
Câu 6. Dẫn khí ethyne qua dung dịch bromine thấy dung dịch bị mất màu. Sản phẩm tạo ra là chất nào
A. CH3-CH2Br B. CH2Br-CH2Br C. CH3-CHBr2 D. CHBr2-CHBr2
Câu 7. Khi cho but-1-ene tác dụng với dung dịch HBr, theo qui tắc Markovnikov sản phẩm nào sau đây là sản phẩm chính ?
A. CH3-CH2-CHBr-CH2Br B. CH3-CH2-CHBr-CH3
C. CH2Br-CH2-CH2-CH2Br D. CH3-CH2-CH2-CH2Br
Câu 8. Chất nào trong 4 chất dưới đây có thể tham gia cả 4 phản ứng: Phản ứng cháy trong oxygen, phản ứng cộng bromine, phản ứng cộng hydrogen (xúc tác Ni, to), phản ứng thế với dung dịch AgNO3 /NH3 ?
A. ethane. B. ethylene. C. acetylene. D. propene
Câu 9. Cho phản ứng: C2H2 + H2O$\xrightarrow{{{t^0},\,xt}}$ A
A là chất nào dưới đây ?
A. CH2=CHOH. B. CH3CHO. C. CH3COOH. D. C2H5OH.
Câu 10. Dãy đồng đẳng của benzene (gồm benzene và alkylbenzene) có công thức chung là
A. CnH2n+6 (n ⩾6). B. CnH2n-6 (n ⩾ 3). C. CnH2n-8 (n ⩾ 8). D. CnH2n-6 (n ⩾ 6).
Câu 11. Tên gọi khác của toluene là
A. o-x ylene. B. Ethylbenzene. C. Methylbenzene. D. Cumene.
Câu 12. Phản ứng của benzene với các chất nào sau đây gọi là phản ứng nitro hóa?
A. HNO3 đậm đặc. B. HNO3 đặc/H2SO4 đặc.
C. HNO3 loãng/H2SO4 đặc. D. HNO2 đặc/H2SO4 đặc.
Câu 13. Để phân biệt benzene, toluene, styrene ta chỉ dùng 1 thuốc thử duy nhất là
A. dung dịch bromine. B. Br2 (xúc tác FeBr3).
C. dung dịch KMnO4. D. dung dịch Br2 hoặc dung dịch KMnO4.
Câu 14. Carbon tetrachloride được dùng làm dung môi trong phòng thí nghiệm và trong công nghiệp do có khả năng hòa tan nhiều chất hữu cơ. Công thức phân tử của carbon tetrachloride là
A. CCl4. B. CHCl3. C. CH2Cl2. D. CH3Cl.
Câu 15. Tên thường của CH3Br là
A. methyl bromide. C. methane bromide.
B. ethyl bromide. D. ethane bromide.
Câu 16. Trước đây, 1,2,3,4,5,6-hexachlorocyclohexane đã từng được dùng rộng rãi làm thuốc diệt muỗi, thuốc trừ sâu,…. Công thức phân tử của 1,2,3,4,5,6-hexachlorocyclohexane là
A. C6H5Cl. B. C6H6Cl6. C. C2H2Cl2. D. C8H8Cl2.
Câu 17. Trong các dẫn xuất halogen của hydrocarbon sau, dẫn xuất nào khi đun nóng với dung dịch NaOH trong dung môi alcohol thu được hai alkene đồng phân?
A. 1-bromobutane. B. chloroethane.
C. 1,3-dichlorobenzene. D. 2-chlorobutane.
Câu 18. Hydrocarbon Y có công thức cấu tạo:
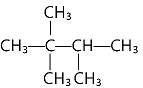
Danh pháp IUPAC của Y là
A. 2,3,3-methylbutane. B. 2,2,3-dimethylbutane.
C. 2,2,3-trimethylbutane. D. 2,3,3-trimethylbutane.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ Câu 1 đến Câu 4. Trong mỗi ý a), b), c), d) ở mỗi Câu, thí sinh chọn đúng hoặc sai.
Câu 1. Chỉ số octane (octane number) là đại lượng đặc trưng cho yếu tố đo lường khả năng chống kích nổ của một nhiên liệu khi nhiên liệu này bốc cháy với không khí bên trong xi lanh của động cơ đốt trong. Nếu chỉ số octane của một mẫu xăng thấp, xăng sẽ tự cháy mà không do bu-gi bật tia lửa điện đốt. Điều này làm cho hiệu suất động cơ giảm và sẽ hư hao các chi tiết máy.
Người ta quy ước rằng chỉ số octane của 2,2,4-trimethylpentane là 100 và của heptane là 0. Các hydrocarbon mạch vòng và mạch phân nhánh có chỉ sô octane cao hơn hydrocarbon mạch không phân nhánh. Để xác định chỉ số octane của một mẫu xăng, người ta dùng máy đo chỉ số octane.
a. Chỉ số octane càng cao, độ chịu nén trước khi phát nổ của xăng càng lớn nên chất lượng xăng càng tốt.
b. Tuỳ vào tỉ số nén của động cơ để chọn xăng phù hợp. Động cơ có tỉ số nén thấp thì không cần dùng xăng có chỉ số octane cao.
c. Xăng không chỉ gồm 2,2,4-trimethylpentane và heptane.
d. Xăng RON 95 có chỉ số octane cao hơn xăng RON 92.
Câu 2. Khí thải của động cơ có thể chứa những chất nào gây ô nhiễm môi trường nên cần những giải pháp nào để hạn chế ô nhiễm môi trường do khí thải của động cơ.
a. Đưa chất xúc tác vào ống xả của động cơ. Nhờ có chất xúc tác, alkane trong khí thải tiếp tục được chuyển hóa thành carbon dioxide và nước, trong khi carbon monoxide và các oxide của nitrogen được chuyển hóa thành carbon dioxide và nitrogen.
b. Sử dụng nhiên liệu cháy sạch: nhiên liệu đảm bảo nghiêm ngặt về chỉ số octane và cetane.
c. Sử dụng nhiên liệu sinh học như xăng pha thêm ethanol (E5, E10,…), biodiesel.
d. Sử dụng các phương tiện giao thông tiết kiệm năng lượng và chuyển đổi sang các loại động cơ điện.
Câu 3. Cho phương trình đốt cháy C2H4 và C2H2:
C2H4 (g) + 3O2 (g) $\xrightarrow{{{t^0}}}$2CO2 (g) + 2H2O (g) ${\Delta _r}H_{298}^0 = – 1411kJ$
2C2H2 (g) + 5O2 (g) $\xrightarrow{{{t^0}}}$4CO2 (g) + 2H2O (g) ${\Delta _r}H_{298}^0 = – 2602kJ$
a. Đốt cháy 1 mol C2H4 thì lượng nhiệt tỏa ra là 1411 kJ.
b. Đốt cháy 1 mol C2H2 thì lượng nhiệt tỏa ra là 2620 kJ.
c. C2H4 và C2H2 được sử dụng trong đèn xì oxygen – acetylene.
d. Không được dùng nước dập tắt đám cháy có mặt đất đèn (có thành phần chính là CaC2).
Câu 4. Cho các hydrocarbon sau: ethane, ethylene, acetylene, butane, benzene, styrene và naphthalene.
a. Ethane, ethylene, acetylene và butane là những chất khí.
b. benzene, styrene và naphtalene là những chất lỏng.
c. Có 2 chất có thể làm mất màu dung dịch KMnO4 ở nhiệt độ thường.
d. Có 1 chất tác dụng với dung dịch AgNO3 trong NH3 ở điều kiện thường.
PHẦN III: Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ Câu 1 đến Câu 6.
Câu 1. Hợp chất C5H10 có bao nhiêu đồng phân alkene?
Câu 2. Cho các alkene sau: CH2=CH-CH3; (CH3)2C=C(CH3)2, CH3CH=CHCH3 và CH3CH=CHC2H5. Có bao nhiêu alkene có đồng phân cis-trans?
Câu 3. Cục Quản Lí Thực Phẩm và Dược Phẩm Hoa Kì (FDA) đã công nhận ethylene là an toàn trong việc kích thích trái cây mau chín. Tuy nhiên khi vượt quá nồng độ cho phép, ví dụ đối với nồng độ 27 000 ppm, tức gấp khoảng 200 lần mức cần thiết để kích thích quá trình chín, một tia lửa điện có thể đốt cháy ethylene và gây ra vụ nổ chết người.
Trong phòng ủ chín, ethylene được sử dụng ở nồng độ 100 ppm – 150 ppm. Khối lượng ethylene cần thiết sử dụng để phòng ủ chín có thể tích 50 m3 đạt nồng độ 140 ppm ở 25 °C và 1 bar là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
Câu 4. Một bình gas sử dụng trong hộ gia đình X có chứa 12 kg khí hóa lỏng (LPG) gồm propane và butane với tỉ lệ mol tương ứng là 2: 3. Khi đốt cháy hoàn toàn, 1 mol propane tỏa ra lượng nhiệt là 2220 kJ và 1 mol butane tỏa ra lượng nhiệt là 2850 kJ. Trung bình, lượng nhiệt tiêu thụ từ đốt khí gas của hộ gia đình X là 10000 kJ/ngày và sau 45 ngày gia đình X dùng hết bình gas trên. Hiệu suất sử dụng nhiệt của hộ gia đình X là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
Câu 5. Tính khối lượng chlorbenzen thu được khi cho 15,6 gam benzene tác dụng vừa đủ với Cl2 theo tỉ lệ mol 1:1 (có mặt FeCl3, t0); biết hiệu suất phản ứng đạt 80%. (Làm tròn kết quả đến hàng phần mười).
Câu 6. Calcium carbide hay đất đèn là một hợp chất vô cơ có công thức CaC2. Nếu có 20 gam một mẩu CaC2 (có lẫn tạp chất trơ) tác dụng với nước dư thu được 7,437 lít khí acetylene (đkc). Cho rằng phản ứng xảy ra hoàn toàn. Độ tinh khiết của mẩu CaC2 là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN
PHẦN I (4,5 đ). Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ Câu 1 đến câu 18. Mỗi Câu hỏi thí sinh chỉ chọn một phương án. Mỗi Câu trả lời đúng thí sinh được 0,25 đ
| 1 | 2 | 3 | 4 | 5 | 6 |
| C | B | B | C | D | D |
| 7 | 8 | 9 | 10 | 11 | 12 |
| B | C | B | D | C | B |
| 13 | 14 | 15 | 16 | 17 | 18 |
| C | A | A | B | D | C |
PHẦN II (4 đ). Câu trắc nghiệm đúng sai. Thí sinh trả lời từ Câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi Câu, thí sinh chọn đúng hoặc sai.
-Điểm tối đa của 01 Câu hỏi là 1 điểm
-Thí sinh lựa chọn chính xác 01 ý trong 1 Câu hỏi được 0,1 điểm
-Thí sinh lựa chọn chính xác 02 ý trong 1 Câu hỏi được 0,25 điểm
-Thí sinh lựa chọn chính xác 03 ý trong 1 Câu hỏi được 0,5 điểm
-Thí sinh lựa chọn chính xác 04 ý trong 1 Câu hỏi được 1 điểm
| Câu | Lệnh hỏi | Đáp án (Đ/S) |
Câu | Lệnh hỏi | Đáp án (Đ/S) |
| 1 | a | Đ | 3 | a | Đ |
| b | Đ | b | S | ||
| c | S | c | S | ||
| d | Đ | d | Đ | ||
| 2 | a | Đ | 4 | a | S |
| b | Đ | b | Đ | ||
| c | Đ | c | Đ | ||
| d | Đ | d | S |
PHẦN III (1,5 đ): Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ Câu 1 đến câu 6. Mỗi Câu đúng 1,5 điểm. Mỗi Câu trả lời đúng thí sinh được 0,25 điểm
| Câu | 1 | 2 | 3 | 4 | 5 | 6 |
| ĐA | 6 | 2 | 7,9 | 75,6 | 18,0 | 96,0 |
HƯỚNG DẪN GIẢI
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ Câu 1 đến Câu 4. Trong mỗi ý a), b), c), d) ở mỗi Câu, thí sinh chọn đúng hoặc sai.
Câu 4. Cho các hydrocarbon sau: ethane, ethylene, acetylene, butane, benzene, styrene và naphthalene.
a. Ethane, ethylene, acetylene và butane là những chất khí. →Đ
b. benzene, styrene và naphtalene là những chất lỏng. →S
c. Có 2 chất có thể làm mất màu dung dịch KMnO4 ở nhiệt độ thường. →S
d. Có 1 chất tác dụng với dung dịch AgNO3 trong NH3 ở điều kiện thường. →Đ
Hướng dẫn giải
b. naphtalene là chất rắn
c. Có 3 chất có thể làm mất màu dung dịch KMnO4 ở nhiệt độ thường: ethylene, acetylene
styrene
d. Có 1 chất tác dụng với dung dịch AgNO3 trong NH3 ở điều kiện thường: acetylene
PHẦN III: Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ Câu 1 đến Câu 6.
Câu 1. Hợp chất C5H10 có bao nhiêu đồng phân alkene?
ĐÁP ÁN LÀ 6
Câu 2. Cho các alkene sau: CH2=CH-CH3; (CH3)2C=C(CH3)2, CH3CH=CHCH3 và CH3CH=CHC2H5. Có bao nhiêu alkene có đồng phân cis-trans?
ĐÁP ÁN LÀ 2
Câu 3. Cục Quản Lí Thực Phẩm và Dược Phẩm Hoa Kì (FDA) đã công nhận ethylene là an toàn trong việc kích thích trái cây mau chín. Tuy nhiên khi vượt quá nồng độ cho phép, ví dụ đối với nồng độ 27 000 ppm, tức gấp khoảng 200 lần mức cần thiết để kích thích quá trình chín, một tia lửa điện có thể đốt cháy ethylene và gây ra vụ nổ chết người.
Trong phòng ủ chín, ethylene được sử dụng ở nồng độ 100 ppm – 150 ppm. Khối lượng ethylene cần thiết sử dụng để phòng ủ chín có thể tích 50 m3 đạt nồng độ 140 ppm ở 25 °C và 1 bar là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN LÀ 7,9
Hướng dẫn giải
Thể tích của ethylene cần sử dụng trong phòng ủ chín có thể tích 50 m3 đạt nồng độ 140 ppm:
$V = 50000 \times \frac{{140}}{{{{10}^6}}} = 7\;L$
Số mol của ethylene cần sử dụng trong phòng ủ chín có thể tích 50 m3 đạt nồng độ 140 ppm:
$n = \frac{V}{{24,79}} = \frac{7}{{24,79}}\;mol$
Khối lượng của ethylene cần sử dụng trong phòng ủ chín có thể tích 50 m3 đạt nồng độ 140 ppm:
${m_{{C_2}{H_4}}} = \frac{7}{{24,79}} \times 28 \approx 7,9gam$
Câu 4. Một bình gas sử dụng trong hộ gia đình X có chứa 12 kg khí hóa lỏng (LPG) gồm propane và butane với tỉ lệ mol tương ứng là 2: 3. Khi đốt cháy hoàn toàn, 1 mol propane tỏa ra lượng nhiệt là 2220 kJ và 1 mol butane tỏa ra lượng nhiệt là 2850 kJ. Trung bình, lượng nhiệt tiêu thụ từ đốt khí gas của hộ gia đình X là 10000 kJ/ngày và sau 45 ngày gia đình X dùng hết bình gas trên. Hiệu suất sử dụng nhiệt của hộ gia đình X là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN LÀ 75,6
Hướng dẫn giải
${n_{{C_3}{H_8}}} = 2x;{n_{{C_4}{H_{10}}}} = 3x\xrightarrow{{12\;kg}}44.2x + 58.3x = 12000$
$ \to x = 45,8\;mol $
${Q_{(12\;kg)}} = (2x \cdot 2220 + 3x \cdot 2850) = 594942\;kJ$
Lượng nhiệt sử dụng sau 45 ngày: 10000.45 = 450000 kJ
$ \to HS = (45000/594942) \cdot 100 \approx 75,6\% $
Câu 5. Tính khối lượng chlorbenzen thu được khi cho 15,6 gam benzene tác dụng vừa đủ với Cl2 theo tỉ lệ mol 1:1 (có mặt FeCl3, t0); biết hiệu suất phản ứng đạt 80%. (Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN LÀ 18,0
Hướng dẫn giải
n (benzene) = 15,6 : 78 = 0,2 mol
Viết gọn:
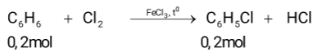
→ m (clobenzen, C6H5Cl) = $0,2 \cdot 112,5 \cdot \frac{{80}}{{100}} = 18,0gam$
Câu 6. Calcium carbide hay đất đèn là một hợp chất vô cơ có công thức CaC2. Nếu có 20 gam một mẩu CaC2 (có lẫn tạp chất trơ) tác dụng với nước dư thu được 7,437 lít khí acetylene (đkc). Cho rằng phản ứng xảy ra hoàn toàn. Độ tinh khiết của mẩu CaC2 là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
ĐÁP ÁN LÀ 96,0
Hướng dẫn giải
CaC2 + 2H2O$ \to $Ca(OH)2 + C2H2
– nC2H2=0,3 mol
– mCaC2=0,3.64=19,2 gam
Độ tinh khiết của mẩu CaC2=.100%=96,0%